|
تضامنًا مع حق الشعب الفلسطيني |
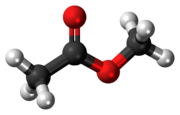
أسيتات الميثيل
| Methyl acetate[1] | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
Methyl acetate |
|
| تسمية الاتحاد الدولي للكيمياء | |
Methyl ethanoate |
|
| أسماء أخرى | |
Methyl ester of acetic acid |
|
| المعرفات | |
| رقم CAS | 79-20-9 |
| بوب كيم (PubChem) | 6584 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C3H6O2 |
| كتلة مولية | 74.08 غ.مول−1 |
| المظهر | Colorless liquid |
| الرائحة | Fragrant, fruity[2] |
| الكثافة | 0.932 g cm−3 |
| نقطة الانصهار | -98 °س، 175 °ك، -144 °ف |
| نقطة الغليان | 56.9 °س، 330 °ك، 134 °ف |
| الذوبانية في الماء | ~25% (20 °C) |
| ضغط البخار | 173 mmHg (20 °C)[2] |
| قابلية مغناطيسية | -42.60·10−6 cm3/mol |
| معامل الانكسار (nD) | 1.361 |
| المخاطر | |
| NFPA 704 |
|
| حدود الاشتعال | 3.1%-16%[2] |
| حد التعرض المسموح به U.S | TWA 200 ppm (610 mg/m3)[2] |
| LD50 | 3700 mg/kg (oral, rabbit)[3] |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
أسيتات الميثيل ، والمعروفة أيضًا باسم MeOAc ، أو استر ميثيل حمض أسيتيك أو إيثانوات الميثيل ، هي إستر الكربوكسيل مع الصيغة CH3COOCH3. وهو عبارة عن سائل قابل للاشتعال مع رائحة لطيفة مميزة تذكرنا ببعض مواد الغراء ومزيلات طلاء الأظافر. تستخدم أسيتات الميثيل في بعض الأحيان كمذيب ، وتكون ضعيفة قطبية و محبة للدهون ، ولكن أسيتات الإيثيل النسبي الوثيق هو مذيب أكثر شيوعًا أقل سمية وأقل قابلية للذوبان في الماء. تمتلك أسيتات الميثيل ذوبانية بنسبة 25٪ في الماء عند درجة حرارة الغرفة. عند درجة الحرارة المرتفعة ، تكون قابليتها للذوبان في الماء أعلى بكثير. أسيتات الميثيل غير مستقرة في وجود قواعد مائية قوية أو أحماض مائية.[4]
التحضير والتفاعلات
يتم إنتاج أسيتات الميثيل صناعيًا عن طريق كربونيل الميثانول كمنتج ثانوي لإنتاج حمض الأسيتيك.[5] تنشأ أسيتات الميثيل أيضا عن طريق الأسترة لحمض الأسيتيك مع الميثانول في وجود أحماض قوية مثل حمض الكبريتيك. عملية الإنتاج هذه مشهورة بسبب عملية مكثفة لإستمان كوداك باستخدام التقطير التفاعلي.
تفاعلات
في وجود قواعد قوية مثل هيدروكسيد الصوديوم أو الأحماض القوية مثل حمض الهيدروكلوريك أو حامض الكبريتيك ، يتم تحللها مرة أخرى إلى ميثانول وحمض أسيتيك ، خاصة عند درجة الحرارة المرتفعة. إن تحويل أسيتات الميثيل إلى مكوناته ، بواسطة حمض ، هو تفاعل من الدرجة الأولى بالنسبة للإستر. إن تفاعل أسيتات الميثيل وقاعدة ، على سبيل المثال هيدروكسيد الصوديوم ، هو تفاعل من الدرجة الثانية بالنسبة لكل من المتفاعلات.
تطبيقات
الاستخدام الرئيسي لأسيتات الميثيل هو كمذيب منخفض السمية متقلبة في المواد اللاصقة ، الدهانات ، ومزيلات طلاء الأظافر.
يتم إنتاج أنهيدريد الخل من خلال استخلاص كربونات من أسيتات الميثيل في عملية مستوحاة من تخليق حامض الخليك في مونسانتو [6]
.
انظر أيضا
مراجع
- ^ فهرس ميرك, 12th Edition, 6089.
- ^ أ ب ت ث "NIOSH Pocket Guide to Chemical Hazards #0391". المعهد الوطني للسلامة والصحة المهنية (NIOSH).
- ^ "Methyl acetate". Immediately Dangerous to Life and Health. المعهد الوطني للسلامة والصحة المهنية (NIOSH).
- ^ Zeno, W. Wicks, JR, Frank N. Jones, S. Peter Pappas, and Douglas A. Wicks (2007). Organic Coatings. Hoboken, New Jersey: Wiley. ISBN:978-0-471-69806-7.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Hosea Cheung, Robin S. Tanke, G. Paul Torrence “Acetic Acid” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. دُوِي:10.1002/14356007.a01_045
- ^ Zoeller, J. R.؛ Agreda, V. H.؛ Cook, S. L.؛ Lafferty, N. L.؛ Polichnowski, S. W.؛ Pond, D. M. (1992). "Eastman Chemical Company Acetic Anhydride Process". Catalysis Today. ج. 13: 73–91. DOI:10.1016/0920-5861(92)80188-S.
| في كومنز صور وملفات عن: أسيتات الميثيل |