|
تضامنًا مع حق الشعب الفلسطيني |
موتر عصبي
| Neurotensin/neuromedin N precursor | |
|---|---|
| معرف | |
| رمز | Pro-NT_NN |
| قاعدة بيانات عوائل البروتينات | PF07421 |
| إنتربرو | IPR008055 |
| قاعدة بيانات توجهات البروتينات في الأغشية | 257 |
| قاعدة بيانات توجهات البروتينات في الأغشية | 2oyv |
| موتر عصبي | |
|---|---|
| المعرفات | |
| رقم CAS | 39379-15-2 |
| بوب كيم (PubChem) | 16133836 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| الصيغة الجزيئية | C78H121N21O20 |
| الكتلة المولية | 1672.92 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
الموتر العصبي هو ببتيد عصبي مكون من 13 حمض أميني مسؤول عن تنظيم إفراز الهرمون المنشط للجسم الأصفر والبرولاكتين بالإضافة إلى دوره التفاعلي الكبير مع النظام دوباميني الفعل. أمكن عزل الموتر العصبي بنجاح للمرة الأولى من مستخلصات تحت المهاد البقري بالاستناد إلى قدرته على إحداث توسيع وعائي مرئي في المناطق الجلدية المكشوفة لدى الجرذان المخدرة.[1]
يتوزع الموتر العصبي في جميع أنحاء الجهاز العصبي المركزي، مع تركز أعلى مستويات له في منطقة تحت المهاد، واللوزة الدماغية والنواة المتكئة. يحرض الموتر العصبي مجموعة من التأثيرات المتنوعة، بما في ذلك تسكين الألم، وانخفاض درجة الحرارة وزيادة النشاط التحركي. يشارك الموتر العصبي أيضًا في تنظيم مسارات الدوبامين. في المناطق المحيطية، يوجد الموتر العصبي في الخلايا الصماوية المعوية للأمعاء الدقيقة، حيث يؤدي عند إفرازه إلى تقلص الأمعاء الدقيقة.[2]
التسلسل والتخلق الحيوي
يتميز الموتر العصبي بتشابه تسلسلي كبير في أحماضه الأمينية ذات النهايات الكربوكسيلية مع العديد من الببتيدات العصبية الأخرى، بما في ذلك نيوروميدين «إن» (المشتق من نفس السلائف). تُعد منطقة النهاية الكربوكسيلية هذه مسؤولة عن النشاط الحيوي الكامل، إذ يلعب جزء النهاية الأمينية دورًا تعديليًا. يمكن أيضًا معالجة سلائف نيوروميدين «إن» / الموتر العصبي من أجل إنتاج ببتيدات كبيرة مكونة من 125-138 حمض أميني مع تسلسلات الموتر العصبي أو نيوروميدين «إن» في نهايتها الكربوكسيلية. من الواضح أن هذه الببتيدات الكبيرة أقل فعالية من نظيراتها الأصغر، لكنها أيضًا أقل حساسية للتحلل ومن شأنها تمثيل منشطات طويلة الأمد داخلية المنشأ في عدد من الحالات الفيزيولوجية المرضية.[3]
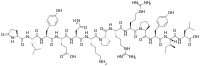
أمكن تحديد تسلسل الموتر العصبي البقري على أنه حمض بيروغلوتامين – ليوسين – تيروسين – غلوتامين – أسبرجين – لايسين – برولين – أرجنين – أرجنين – برولين – تيروسين – إيزوليوسين – ليوسين – هيدروكسيد. يمكن تصنيع الموتر العصبي كجزء من بروتين السلف المكون من 169 أو 170 حمض أميني الذي يحتوي بدوره على الببتيد العصبي نيوروميدين «إن» ذي الصلة. تتوضع مجالات التشفير الببتيدية بشكل ترادفي بالقرب من طرف النهاية الكربوكسيلية للسلائف بالإضافة إلى ربطها وفصلها بواسطة مواقع معالجة الأحماض الأمينية الأساسية المزدوجة (لايسين – أرجنين).[4][5]
التعبير الجيني
من المثبت أن التعبير الجيني للموتر العصبي خاضع لعملية التعديل بواسطة الإستروجين في مستنبتات خلايا الورم الأرومي العصبي «إس كيه – إن – إس إتش» لدى الإنسان والفئران على حد سواء من خلال التفاعلات مع إشارات أحادي فوسفات الأدينوسين الحلقي (سي إيه إم بّي). على وجه التحديد، يعمل الإستروجين على زيادة كل من نشاط أحادي فوسفات الأدينوسين الحلقي وفسفرة البروتين المرتبط بعنصر استجابة أحادي فوسفات الأدينوسين الحلقي في خلايا الورم الأرومي العصبي قبل تحريض النسخ الجيني للموتر العصبي. بالإضافة إلى ذلك، تحدث إعاقة في النسخ الجيني للموتر العصبي لدى الفئران معطلة الجين المفتقرة إلى الوحدة الفرعية «آر آي آي بيتا» من الإنزيم الكامل لبروتين كيناز ألفا. قد تشير هذه النتائج إلى وجود آليات تداخل الإشارات في النشاط الهرموني الدماغي والتعبير عن الجينات المرتبطة بالهرمونات. ارتبطت التغيرات الأخرى ذات الصلة بالهرمونات الجنسية في تعبير الموتر العصبي مع نشاط الباحة أمام التصالبة البصرية. أظهر تعبير الموتر العصبي لدى أناث الجرذان أعلى مستوى له في الباحة أمام التصالبة البصرية الإنسية (إم بّي أو إيه) خلال طور مقدمات الوداق من الدورة الوداقية.[6]
ظهر تعبير معدل لجينات الموتر العصبي بالإضافة إلى جينات مستقبلات الموتر العصبي خلال فترة ما بعد الولادة لدى إناث الفئران. بينما انخفضت مستويات الرنا المرسال لمستقبل الموتر العصبي 1 (إن تي إس آر 1) في النواة الوطائية المجاورة للبطين (بّي في إن)، أظهر الموتر العصبي، دونًا عن الرنا المرسال للموتر العصبي، مستويات أعلى في النواة الوطائية المجاورة للبطين. ارتفع مستوى التعبير عن الرنا المرسال للموتر العصبي فضلًا عن الببتيد نفسه في الباحة أمام التصالبة الإنسية (إم بّي أو إيه). لم تظهر هذه الأنماط من التعبير في مجموعة الإناث المضبوطة العذراء، وتتوافق الأنماط التعبيرية هذه مع الأبحاث الأخرى التي تشير إلى تباين التعبير الجيني للموتر العصبي في تنظيم السلوكيات الأمومية.[7]
أظهرت أنماط تعبير الموتر العصبي الأخرى المتعلقة بالباحة أمام التصالبة الإنسية ارتباطًا بتعديل المكافأة الاجتماعية. كشف تحليل العصبونات الموسومة بجين الموتر العصبي أن الامتدادات العصبونية الحاوية على الموتر العصبي من الباحة أمام التصالبة الإنسية إلى المنطقة السقيفية البطنية (في تي إيه) لدى الفئران مرتبطة مع تشفير إشارات الرائحة بالإضافة على الانجذاب الاجتماعي، ما يشير بدوره إلى دور الموتر العصبي الهرموني والمشارك في إشارات المكافأة على حد سواء.[8]
يلعب الموتر العصبي أيضًا دورًا في عمليات معالجة التعلم. أظهرت إحدى الدراسات التي اختبرت تطور الأغنية لدى شرشوريات الزيبرا وجود تباينات في التعبير الجيني للموتر العصبي ولمستقبل الموتر العصبي عبر المراحل المختلفة من تطور الأغنية. اتسمت المرحلة المبكرة من الانتقال بين الفترتين الحسية والحسية الحركية بانخفاضات في التعبير عن الرنا المرسال للموتر العصبي ومستقبل الموتر العصبي على حد سواء، ما من شأنه الإشارة إلى دور الموتر العصبي في بدء التعلم الحسي الحركي. خلال مرحلة الأغنية الفرعية الحسية الحركية، يظهر كل من التعبير الجيني للموتر العصبي والتعبير الجيني لمستقبل الموتر العصبي 1 (إن تي إس آر 1) أنماطًا تعبيرية تكميلية في مناطق الدماغ المرتبطة بالأغنية، ما قد يشير إلى تغيرات في الاستجابات العصبونية للموتر العصبي عبر مراحل التطور.[9]
يلعب الموتر العصبي أيضًا دورًا في النسج المحيطية خارج الجهاز العصبي، بشكل رئيسي في السبيل الهضمي، بالإضافة إلى مشاركته في تطور السرطان. ثبت وجود دور لمثيلة محفز الدنا كمنظم رئيسي للتعبير عن جينات مستقبل الموتر العصبي 1 و2 في الخلايا السرطانية القولونية المستقيمية. بالإضافة إلى ذلك، أدى تعطيل جين «إن تي إس آر 1» والعلاج باستخدام مناهضة «إن تي إس آر 1» إلى تثبيط تكاثر الخلايا السرطانية القولونية المستقيمية وهجرتها. ارتبط كل من الورم العضلي الأملس والأورام الليفية في نسج الرحم مع ارتفاع التعبير عن الموتر العصبي وجين «إن تي إس آر 1».[10]
المراجع
- ^ Carraway R، Leeman SE (1973). "The isolation of a new hypotensive peptide, neurotensin, from bovine hypothalami". J. Biol. Chem. ج. 248 ع. 19: 6854–61. DOI:10.1016/S0021-9258(19)43429-7. PMID:4745447. مؤرشف من الأصل في 2023-04-28.
- ^ Friry C، Feliciangeli S، Richard F، Kitabgi P، Rovere C (فبراير 2002). "Production of recombinant large proneurotensin/neuromedin N-derived peptides and characterization of their binding and biological activity". Biochem. Biophys. Res. Commun. ج. 290 ع. 4: 1161–8. DOI:10.1006/bbrc.2001.6308. PMID:11811984.
- ^ Carraway R، Leeman SE (1975). "The amino acid sequence of a hypothalamic peptide, neurotensin". J. Biol. Chem. ج. 250 ع. 5: 1907–11. DOI:10.1016/S0021-9258(19)41780-8. PMID:1167549.
- ^ Dobner PR، Barber DL، Villa-Komaroff L، McKiernan C (1987). "Cloning and sequence analysis of cDNA for the canine neurotensin/neuromedin N precursor". Proc. Natl. Acad. Sci. U.S.A. ج. 84 ع. 10: 3516–20. Bibcode:1987PNAS...84.3516D. DOI:10.1073/pnas.84.10.3516. PMC:304902. PMID:3472221.
- ^ Kislauskis E، Bullock B، McNeil S، Dobner PR (1988). "The rat gene encoding neurotensin and neuromedin N. Structure, tissue-specific expression, and evolution of exon sequences". J. Biol. Chem. ج. 263 ع. 10: 4963–8. DOI:10.1016/S0021-9258(18)68881-7. PMID:2832414.
- ^ Kinkead, B, Dobner PR, Egnatashvili, V, Murray, T, Deitemeyer, N, Nemeroff, CB (2005). "Neurotensin-deficient mice have deficits in prepulse inhibition: restoration by clozapine but no haloperidol, olanzapine, or quetiapine". J. Pharmacol. Exp. Ther. ج. 315 ع. 1: 256–264. DOI:10.1124/jpet.105.087437. PMID:15987829. S2CID:15095566. مؤرشف من الأصل في 2023-04-28.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Katz LM، Young A، Frank JE، Wang Y، Park K (مارس 2004). "Neurotensin-induced hypothermia improves neurologic outcome after hypoxic-ischemia". Crit. Care Med. ج. 32 ع. 3: 806–10. DOI:10.1097/01.CCM.0000114998.00860.FD. PMID:15090966. S2CID:41533372.
- ^ Dobner, PR, Fadel, J, Deitemeyer, N, Carraway, RE, Deutch, AY (2001). "Neurotensin-deficient mice show altered responses to antipsychotic drugs". Proc. Natl. Acad. Sci. USA. ج. 98 ع. 14: 8048–8053. Bibcode:2001PNAS...98.8048D. DOI:10.1073/pnas.141042198. PMC:35465. PMID:11427716.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Smith، Matthew J.؛ Wise، Phyllis M. (1 يوليو 2001). "Neurotensin Gene Expression Increases during Proestrus in the Rostral Medial Preoptic Nucleus: Potential for Direct Communication with Gonadotropin-Releasing Hormone Neurons*". Endocrinology. ج. 142 ع. 7: 3006–3013. DOI:10.1210/endo.142.7.8256. ISSN:0013-7227. PMID:11416022.
- ^ Watters, Jyoti J.; Dorsa, Daniel M. (1 Sep 1998). "Transcriptional Effects of Estrogen on Neuronal Neurotensin Gene Expression Involve cAMP/Protein Kinase A-Dependent Signaling Mechanisms". Journal of Neuroscience (بEnglish). 18 (17): 6672–6680. DOI:10.1523/JNEUROSCI.18-17-06672.1998. ISSN:0270-6474. PMC:6792960. PMID:9712639.
روابط خارجية
- Neurotensin في المكتبة الوطنية الأمريكية للطب نظام فهرسة المواضيع الطبية (MeSH).