|
تضامنًا مع حق الشعب الفلسطيني |
تاريخ علم الجينات
تاريخ علم الجينات |
| جزء من سلسلة مقالات عن |
| علم الوراثة |
|---|
 |
بدأ تاريخ علم الوراثة مع عمل الراهب أغسطينوس جريجور يوهان مندل. الذي وصف عمله على نباتات البازلاء، وقام بنشره في عام 1866، وهو ما أصبح يعرف فيما بعد باسم الوراثة المندلية. كثير من نظريات الوراثة انتشرت في القرون التي سبقت مندل ولعدة عقود بعد عمله.
تميزت سنة 1900 بـ «إعادة اكتشاف مندل» على يد كل من هوغو دي فريس، وكارل كورنس وإريك فون تشرماك، وبحلول سنة 1915 تم تطبيق المبادئ الأساسية لعلم الوراثة المندلية على مجموعة واسعة من الكائنات أبرزها ذبابة الفاكهة السوداء البطن. تم تطوير النموذج المندلي بقيادة توماس هانت مورجان وزملائه «المختصين في ذبابة الفاكهة»، وعلماء الهندسة الوراثية، وحظى هذا النموذج الجديد بقبول واسع بحلول عام 1925. إلى جانب العمل التجريبي، وضع علماء الرياضيات الإطار الإحصائي لعلم الوراثة السكانية، وبذلك تدخلت التفسيرات الوراثية في دراسة التطور.
مع ظهور الأنماط الأساسية من الوراثة الجينية، تحول العديد من علماء الأحياء للبحث حول الطبيعة الفيزيائية للجين. في العقد 1940 وفي وقت مبكر من 1950، أشارت التجارب إلى الحمض النووي باعتباره جزء من الصبغيات (وربما بروتينيات النواة الأخرى) التي تمسك بالجينات. التركيز على نموذج جديد من الكائنات مثل الفيروسات والبكتيريا، جنبا إلى جنب مع اكتشاف الهيكل الحلزوني المزدوج للحمض النووي في عام 1953، ميّز مرحلة التحول إلى عصر علم الوراثة الجزيئي.
في السنوات التالية، وضع الكيميائيون تقنيات التسلسل لكل من الأحماض النووية والبروتينات، فيما عمل آخرون على العلاقة بين شكلين من الجزيئات البيولوجية: الشفرة الوراثية. أصبح تنظيم التعبير الجيني قضية مركزية في العقد 1960. من 1970 كان يمكن السيطرة علي التعبير الجيني والتلاعب فيه عن طريق الهندسة الوراثية. في العقود الأخيرة من القرن العشرين، ركز العديد من علماء الأحياء على مشاريع وراثية ذات نطاق واسع، والبحث حول تسلسل الجينوم بأكمله.
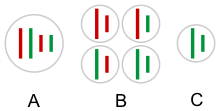
الأفكار السابقة لمندل حول الوراثة
النظريات القديمة
كانت النظريات المبكرة الأكثر تأثيرا حول الوراثة ترجع إلى أبقراط وأرسطو. كانت نظرية أبقراط (التي ربما بُنيت على تعاليم أنكساغوراس) مشابهة لأفكار داروين في وقت لاحق عن شمولية التخلق، حيث تشمل المواد الوراثة التي تجتمع من جميع أنحاء الجسم. اقترح أرسطو بدلا من ذلك أن المبدأ الذي يمنح الكائن الحي شكله ينتقل عن طريق السائل المنوي (الذي اعتبره شكل منقى للدم) ودم حيض الأم، وأن هذه المواد تفاعلت في الرحم لتوجيه النمو المبكر للكائن الحي. بالنسبة لكل من أبقراط وأرسطو وتقريبا كل علماء الغرب حتى أواخر القرن ال19 فإن توريث الصفات المكتسبة كان يعتبر حقيقة راسخة بحيث أن أي نظرية وراثية مقبولة يجب أن تشرحها. في الوقت نفسه، اتخذت الفصائل الفردية جوهر ثابت لها. بحيث تمر فقط بتغيرات وراثية سطحية.[1]
في تشاركا سامهيتا من عام 300 ميلاديا، رأى كتّاب الطب القدامى في الهند أن خصائص الطفل تتحدد من خلال أربعة عوامل: (1) المواد الإنجابية للأم، (2) الحيوانات المنوية للأب، (3) بعضها من النظام الغذائي للأم الحامل (4) الأشخاص المرافقين للروح التي تدخل في الجنين. كل من هذه العوامل الأربعة كان لها أربعة أجزاء مكونةً ستة عشر عاملا منها الكارما الخاصة بالوالدين والروح التي تحدد السمات السائدة، وهو ما يعطى للطفل خصائصه.[2]
في القرن التاسع عشر الميلادي، اهتم الكاتب العربي الأفريقي الجاحظ بالآثار البيئية على احتمالية الحيوان في البقاء على قيد الحياة.[3] بينما في عام 1000 ميلاديا، كان الطبيب العربي أبو القاسم الزهراوي (المعروف باسم ألبوكاسيس في الغرب) أول طبيب يصف بوضوح الطبيعة الوراثية لمرض عدم تخثر الدم (الهيموفيليا) في كتابه التصريف لمن عجز عن التأليف.[4] في 1140 ميلاديا، وصف يهوذا هاليفي الصفات الوراثية السائدة والمتنحية في كتابه الكوزاري.[5]
النظاميات النباتية والتهجين
في القرن الثامن عشر، مع المعرفة المتزايدة بالتنوع النباتي والحيواني وما صاحبها من زيادة التركيز على علم التصنيف، بدأت أفكار جديدة حول الوراثة في الظهور. أجرى لينيوس وغيره (من بينهم جوزيف غوتليب كولريتور، كارل فريدريش فون غارتنر، وتشارلز ناودين) تجارب مكثفة على التهجين، خصوصا تهجين الأنواع. وصف مُهجّني الأنواع مجموعة واسعة من الظواهر الوراثية، تشمل العقم الهجين والتباين العالي في إعادة التهجين مع أحد الأبوين.[6]
قام مُربّي النباتات بتطوير مجموعة من أصناف مستقرة في كثير من الأنواع النباتية الهامة. في أوائل القرن التاسع عشر، أنشأ أوغستين ساجريت مفهوم الهيمنة، مكتشفا أنه عندما يتم تزاوج بعض أنواع النباتات، بعض الصفات (الموجودة في أحد الوالدين) تظهر عادة في النسل. كما وجد أيضا أن بعض الصفات الموروثة غير الموجودة في أي من الأبوين قد تظهر في النسل. مع ذلك، قام مربي النباتات بمحاولة صغيرة لإقامة الأساس النظري لعملهم أو لتبادل المعرفة التي لديهم مع العمل الحالي لعلم وظائف الأعضاء (الفسيولوجي)، [7] على الرغم من قيام مربي نباتات جارتونز الزراعية في انجلترا بتوضيح نظامهم.
مندل
في تجارب التناسل بين 1856 و 1865، قام جريجور مندل أولا بتتبع أنماط توريث صفات معينة في نبات البازلاء، وبيّن أنها تخضع لقواعد إحصائية بسيطة مع كون بعض الصفات مُهيمنة «سائدة» وبعضها الآخر متنحية. أظهرت هذه الأنماط من الوراثة المندلية أن تطبيق الإحصاءات على علم الوراثة يمكن أن يكون مفيدا للغاية. كما أنها تتناقض أيضا مع نظريات القرن التاسع عشر حول الوراثة المختلطة حيث ظلت الصفات مميزة خلال أجيال عديدة من التهجين.[8] ومنذ ذلك الوقت تم تفسير العديد من أشكال الوراثة الأكثر تعقيدا.
توصل مندل من خلال تحليله الإحصائي إلى المفهوم الذي وصفه بأنه «الصفة» (الذي ينطبق أيضا في ذهنه على المحدد لهذه الصفة). استخدم في جملة واحدة فقط من ورقته التاريخية مصطلح «العوامل» للدلالة على «مادة الصانعة» للصفة: «حتى الآن وعلى مدى التجربة، نجد تأكيد على أنه في كل حالة يمكن فقط أن تتكون ذرية ثابتة عندما تحمل الخلية البيضية وحبة اللقاح المخصبة صفة مشابهة، بحيث يقدم كلا منهما المواد اللازمة لخلق جيل من الأفراد المتماثلة تماما، كما هو الحال مع الإخصاب الطبيعي في الأنواع النقية، ولذلك يجب علينا أن نأخذ في الاعتبار حقيقة أنه يجب أن تتوافر عوامل مماثلة للعمل أيضا على إنتاج أشكال ثابتة في النباتات الهجينة.»(مندل، 1866).
نشرت أعمال مندل في عام 1866 باسم (تجارب على تهجين النبات)، (وقائع من جمعية التاريخ الطبيعي في برون)، بعد أن ألقى محاضرتين عن عمله في أوائل 1866 .
ما بعد مندل وما قبل إعادة الاكتشاف
نُشرت أعمال مندل في مجلة علمية مغمورة نسبيا، ولم تحظ بأي اهتمام في الأوساط العلمية. بدلا من ذلك، اندفعت المناقشات حول نماذج الوراثة التي قدمتها نظرية نظرية داروين عن التطور عن طريق الانتقاء الطبيعي، والتي بدا فيها أن آليات الوراثة غير اللاماركية مطلوبة. لم تتلق نظرية داروين الخاصة حول الوراثة، وشمولية التخلق درجة كبيرة من القبول. هناك نسخة أكثر رياضية عن شمولية التخلق، والتي خفضت كثيرا من تماسك النظرية داروين اللاماركية، وُضعت هذه النسخة باعتبارها المدرسة «البيومترية» للوراثة التي كتبها ابن عم داروين، فرانسيس غالتون. على غرار غالتون وخليفته كارل بيرسون، حاولت المدرسة البيومترية بناء النماذج الإحصائية للوراثة والتطور، مع بعض النجاح المحدود ولكن الحقيقي، وإن كانت الطرق الصحيحة للوراثة غير معروفة ولم يكن حولها جدال إلى حد كبير.
في عام 1883 أجرى أوغست وايزمان التجارب على تناسل الفئران التي أزيلت ذيولها جراحيا. أوضحت نتائجه - أن إزالة ذيل الفأر جراحيا لم يكن له تأثير على ذيول ذريته - متحديا بذلك نظريات شمولية التخلق واللاماركية، التي رأت أن التغييرات التي يتعرض لها الكائن الحي خلال فترة حياته يمكن أن تكون موروثة خلال نسله. قدم ايزمان نظرية بلازما الجرثومة للوراثة، التي رأت أن المعلومات الوراثية تُحمل فقط في خلايا الحيوانات المنوية والبويضات.[9]
إعادة اكتشاف مندل
تساءل هوغو دي فريس ما قد تكون طبيعة المادة الوراثية، وعلى وجه الخصوص تساءل ما إذا كانت البلازما الجرثومية مختلطة مثل الطلاء أم لا أو ما إذا كانت المعلومات محمولة في حزم منفصلة التي بقيت دون تكسير. في العقد 1890 كان يقوم بإجراء تجارب التناسل على مجموعة متنوعة من الأنواع النباتية، في عام 1897 نشر ورقة عن نتائجه التي ذكرت أن كل سمة موروثة كان يتحكم بها اثنين من الجزيئات المنفصلة من المعلومات، واحد من كل من الوالدين، وأن هذه الجسيمات تنتقل جنبا إلى جنب سليمة إلى الأجيال الجديدة. في عام 1900 كان يُعِد ورقة أخرى عن المزيد من نتائجه عندما عُرضت عليه نسخة من ورقة مندل 1866 من قبل أحد الأصدقاء الذي اعتقد أنها قد تكون ذات صلة مع عمل دي فريس. مضى قدما ونشر ورقته عام 1900 دون ذكر أسبقية مندل. في وقت لاحق من العام نفسه كان عالم نبات آخر، كارل كورنس، الذي كان قد قام بإجراء تجارب التهجين مع الذرة والبازلاء، يبحث في الأدب عن التجارب ذات الصلة قبل نشر نتائجه الخاصة عندما عثر على ورقة مندل، والتي كانت لها نتائج مماثلة لنتائجه. اتهم كرونس دي فريس بالاستيلاء على مصطلحات من ورقة مندل دون نسب الفضل له أو الاعتراف بأسبقيته. في الوقت نفسه، كان عالم نبات آخر، إريك فون تشرماك يقوم بتجاربه على تناسل نبات البازلاء وتوصل إلى نتائج مماثلة لمندل. اكتشف هو أيضا ورقة مندل خلال بحثه في الأدب عن الأعمال ذات الصلة. في ورقة لاحقة اعترف دي فريس بفضل مندل وبأن عمله هو فقط امتداد لأعمال مندل السابقة.[9]
ظهور علم الوراثة الجزيئية
بعد إعادة اكتشاف عمل مندل كان هناك صراع بين ويليام باتيسون وبيرسون على آلية الوراثة، تم حل هذا الصراع على يد رونالد فيشر في عمله «العلاقة بين الأقارب بناء على فرضية مندل الوراثية».
في عام 1910، أظهر توماس مورغان أن الجينات تتواجد على كروموسومات محددة. ثم أوضح لاحقا أن الجينات تحتل مواقع محددة على الكروموسوم. مع هذه المعرفة، بدأ مورغان وطلابه بوضع خريطة الكروموسومات الأولى لذبابة الفاكهة. في عام 1928، أظهر فريدريك غريفيث أن الجينات يمكن نقلها. فيما يعرف الآن باسم تجربة غريفيث، حيث قام بحقن فأر صغير بسلالة قاتلة من البكتيريا التي كانت قُتلت بالحرارة ثم نقلت معلوماتها الوراثية لسلالة آمنة من نفس البكتيريا، مما أسفر عن موت الفأر.
كشفت سلسلة من الاكتشافات في عقود لاحقة أن المادة الوراثية مصنوعة من الحمض النووي DNA (الحمض النووي الريبي منقوص الأكسجين). في عام 1941، أظهر كلا من جورج بيدل وإدوارد تاتوم أن الطفرات الحادثة في الجينات تسبب أخطاء في خطوات محددة في المسارات الأيضية. أظهر هذا أن جينات معينة ترمز لبروتينات معينة، مما قاد إلى فرضية «جين واحد، إنزيم واحد».[10] أوضح أوزوالد آفري، وكولن مونرو ماكلويد، وماكلين مكارتي في عام 1944 أن الحمض النووي يحمل المعلومات الجينة.[11] في عام 1952، أنتج روزاليند فرانكلين وريمون جوزلينج نمط لافت للنظر من حيود الأشعة السينية الواضحة يُظهر شكل حلزوني، في عام 1953، توصل جيمس واطسون وفرانسيس كريك إلى التركيب الجزيئي للحمض النووي. أنشأت هذه الاكتشافات معا الفكرة المركزية لعلم الأحياء الجزيئية، التي تنص على أن البروتينات يتم ترجمتها من الحمض النووي الريبي RNA الذي نُسخ من الحمض النووي DNA. أظهرت هذه الفكرة ومنذ نشأتها بعض الاستثناءات، مثل النسخ العكسي في الفيروسات القهقرية.
في عام 1972، كان والتر فيرس وفريقه في جامعة غنت أول من قام بتحديد تسلسل الجين: الجين الخاص بالبروتين المُغلِّف لجراثيم MS2.[12] اكتشف كل من ريتشارد روبرتس وفيليب شارب في عام 1977 أن الجينات يمكن تقسيمها إلى شرائح. أدى ذلك إلى ظهور فكرة أن جين واحد يمكنه أن ينتج العديد من البروتينات. هذا النجاح الكبير في التوصل إلى تسلسل الجينوم لكثير من الكائنات الحية أدى إلى تعقد التعريف الجزيئي للجينات. على وجه الخصوص، لا يبدو أن الجينات تنتظم جنبا إلى جنب على الحمض النووي كحبات منفصلة. بدلا من ذلك، قد تتداخل مناطق إنتاج البروتينات المتخصصة على الحمض النووي، بحيث تبرز فكرة أن «الجينات هي اتصال واحد طويل».[13][14] ظهر افتراض لأول مرة في عام 1986 من قبل والتر جيلبرت أنه لا الحمض النووي ولا البروتين سوف يكون مطلوبا في مثل هذا النظام البدائي ذو المرحلة المبكرة جدا من التطور إذ يمكن لـ RNA أن يؤدي ببساطة دور المحفز ومعالج تخزين المعلومات الوراثية.
تُعرف الدراسة الحديثة على علم الوراثة على مستوى الحمض النووي باسم علم الوراثة الجزيئية، كما يُعرف تركيب علم الوراثة الجزيئية مع التطور الدارويني التقليدي باسم التركيب التطوري الحديث.
التاريخ المبكر
1865: ورقة الراهب النمساوي جريجور مندل، تجارب على تهجين النبات.
1868: درس مندل وراثة الصفات بين الأجيال على أساس من تجاربه على نباتات البازلاء. استخلص من تجاربه أن هناك خلاصة مادية على يتم تمريرها بين الأجيال من كلا الوالدين. أنشأ مندل المبادئ الأساسية للوراثة، ألا وهي مبادئ الهيمنة، والتصنيف المستقل، والعزل.
1869: اكتشف فريدريك ميسشر حمض ضعيف في أنوية خلايا الدم البيضاء، وهو ما نسميه اليوم الحمض النووي. في عام 1871 قام بعزل نواة الخلية، حيث فصل الخلايا النووية من العُصابة ثم عالجها مع الببسين (إنزيم يكسر البروتينات). من هذا المنطلق، أعاد كشف المادة الحمضية التي أطلق عليها «نوكلين».[15]
1880 - 1890: أوضح فالتر فليمنغ، وإدوارد استراسبرجر، وإدوارد فان بنيدين توزيع الكروموسومات خلال انقسام الخلية.
1889: قام ريتشارد ألتمان بتنقية الحمض النووي من البروتين. ومع ذلك، فإن الحمض النووي لم يكن نقيا بالقدر الذي افترضه. وقد تقرر في وقت لاحق احتوائه على كمية كبيرة من البروتين.
1889: افترض هوغو دي فريس أن «وراثة سمات محددة في الكائنات يأتي عن طريق الجسيمات»، تسمى هذه الجسيمات «الجينات (العامة)» [16]
1902: اكتشف أرشيبالد غارود الأخطاء الوراثية في الأيض. كان تفسير القشوة (اتحاد جينين غير متماثلين) سمة هامة تميز أبحاث غارود، وإن كان بشكل غير مباشر. عندما درس غارود «آلكابتونوريا»، وهو الاضطراب الذي يجعل البول يتحول إ سريعا إلى اللون الأسود بسبب وجود إنزيم جنتيسيت، ولاحظ أنه منتشر بين الأفراد الذين يرتبط والداهم بقرابة قوية.[17][18][19]
1903: افترض كل من والتر ساتون وتيودور بوفيري بشكل مستقل أن الكروموسومات، التي تنعزل على الطريقة المندلية، هي وحدات الوراثة.[20] كان بوفري يدرس قنافذ البحر عندما وجد أن جميع الكروموسومات في قنافذ البحر يجب أن تكون موجودة ليتم نمو الجنين. كما أظهر عمل ساتون على الجنادب أن الكروموسومات تتواجد في أزواج متماثلة من كروموسومات الأم والأب التي تنفصل أثناء الانقسام الاختزالي.[21] واستنتج أن هذا يمكن أن يكون «الأساس المادي لقانون مندل الوراثي».[22]
1905: وطد ويليام باتيسون مصطلح «علم الوراثة» في رسالة إلى آدم سيدجويك،[23] وخلال اجتماع في عام 1906.[24]
1908: اقترح جي . اتش هاردي، وويلهلم واينبرغ نموذج التوازن هاردي ـ واينبرغ، الذي يصف ترددات الأليلات في الجينات لدى مجموعة من السكان، التي توجد تحت ظروف معينة كثابت، وفي حالة من التوازن من جيل إلى جيل ما لم يتم إدخال التأثيرات محددة مربكة .
1910: أظهر توماس هانت مورجان أن الجينات موجودة على الكروموسومات في حين قام بتحديد طبيعة الصفات المرتبطة بالجنس من خلال دراسة ذبابة الفاكهة. وقرر أن طفرة لون العينين الأبيض كانت صفة مرتبطة بالجنس بناء على المبادئ المندلية في العزل والتصنيف المستقل.[25]
1911: ألفريد استورتفانت، وهو واحد من تلامذة مورغان، اخترع إجراءات تخطيط الربط الذي يعتمد على تكرار إعادة التركيب.[26] وبعد سنوات قليلة، قام ببناء أول خريطة كروموسوم في العالم.[27]
1913: صمم ألفريد استورتفانت الخريطة الجينية الأولى للكروموسوم.
1913: تظهر خرائط الجينات أن الكروموسومات تحتوي على ترتيب خطي للجينات.
1918: نشر رونالد فيشر «الارتباط بين الأقارب بناء على افتراض مندل للوراثة» بادئًا بذلك التركيب الحديث لعلم الوراثة والبيولوجيا التطورية.
1920: بدأت الليسينكووية، ونصت الليسينكووية أن العامل الوراثي لا يوجد فقط في النواة، ولكن أيضا في السيتوبلازم، على أن يسمى البروتوبلازم الحي.[28]
1923: درس فريدريك غريفيث التحول البكتيري ولاحظ أن الحمض النووي يحمل جينات مسؤولة عن الإصابة بالأمراض.[29]
1928: اكتشف فريدريك غريفيث أن المادة الوراثية من البكتيريا الميتة يمكن إدراجها في البكتيريا الحية (انظر تجربة غريفيث)
1931: يتم تعريف العبور على أنه سبب إعادة التركيب. تم تنفيذ أول إظهار خلوي لهذا العبور على يد باربرا مكلينتوك وهارييت كريتون.
1933: استطاع جان براشيه أن يظهر أن الحمض النووي DNA يوجد في الكروموسومات بينما RNA موجود في سيتوبلازم كل الخلايا.
1933: حصل توماس مورغان على جائزة نوبل لرسم خرائط الربط. استطاع عمله شرح الدور الذي يلعبه الكروموسوم في الوراثة.
1941: أوضح إدوارد تاتوم وجورج بيدل أن الجينات ترمز لبروتينات.[30]
1943: تجربة لوريا، ديلبروك: أظهرت هذه التجربة أن الطفرات الوراثية تمنح القدرة على مقاومة الجراثيم التي تنشأ في غياب الاختيار، بدلا من أن تكون ردا على الاختيار.[31]
عصر الحمض النووي DNA
1944: عزل الحمض النووي كمادة وراثية في تجربة أفيري-ماكلويد-مكارتي (الذي سمى وقتها بمبدأ التحويل)[32]
1947: اكتشف سلفادور لوريا إعادة تنشيط الفاج المشع،[33] مما حفز العديد من الدراسات في عمليات إصلاح الحمض النووي في الجراثيم، وغيرها من الكائنات، بما في ذلك البشر.[34]
1948: اكتشاف باربرا مكلينتوك الجينات القافزة (الترانسبوزونات) في نبات الذرة.
1950: حدد أروين تشارجاف طريقة المزاوجة بين القواعد النيتروجينية. درس تشارجاف وفريقه الحمض النووي لكائنات متعددة، وعثروا على ثلاثة أشياء (المعروفة أيضا باسم قواعد تشارجاف). أولا، تركيز البريميدينات (الجوانين والأدينين) توجد دائما بنفس المقدار مساوية لبعضها البعض. ثانيا، تركيز البيورينات (السيتوزين والثيميدين) تكون متساوية دائما. وأخيرا، وجد تشارجاف وفريقه نسبة البريميدينات والبيورينات تتوافق مع بعضها البعض.[35][36]
1952: تجربة هيرشي تشيس أتثبتت أن المعلومات الوراثية في الفاج (وضمنا، جميع الكائنات الأخرى) هي الحمض النووي DNA.[37]
1952: التقطت صورة حيود الأشعة السينية للحمض النووي، بواسطة ريمون جوزلينج في مايو 1952، وهو طالب يشرف عليه روزاليند فرانكلين.[38]
1953: تم كشف بنية الحمض النووي وهي في شكل الحلزون المزدوج على يد جيمس واطسون وفرانسيس كريك.[39] 1955: قام ألكسندر تود بتحديد التركيب الكيميائي للقواعد النيتروجينية. قام تود أيضا بتصنيع أدينوسين ثلاثي الفوسفات (ATP) وفلافين ثنائي النوكليوتيد الأدينين (FAD) بنجاح. وحصل على جائزة نوبل في الكيمياء عام 1957 لإسهاماته في المعرفة العلمية للنيوكليوتيدات والانزيمات المساعدة للنيوكليتدات.[40] 1955: بينما كان جو هين تجيو يعمل في مختبر ألبرت ليفان، حدد عدد الكروموسومات في البشر ليكون 46 كروموسوم. كان تجيو يحاول صقل تقنية قائمة لفصل الكروموسومات على الشرائح الزجاجية عن طريق إجراء دراسة أنسجة الرئة الجنينية البشرية، عندما رأى أن هناك 46 كروموسوم بدلا من 48. وهو الاكتشاف الذي شكل ثورة في علم الوراثة الخلوية.[41]
1957: قام آرثر كورنبرغ وسيفيرو أوتشوا بتوليف الحمض النووي في أنبوب اختبار بعد اكتشاف الوسائل التي يتضاعف بها الحمض النووي. وفر بوليميريز الحمض النووي 1 متطلبات تركيب الحمض النووي في المختبر. مُنح كورنبرغ وأوتشوا جائزة نوبل في عام 1959 لهذا العمل.[42][43]
1957/1958: اقترح كلا من روبرت هولي، مارشال نيرنبرج، هار غوبند خورانا تسلسل النوكليوتيدات في جزيء الحمض الريبي النووي النقال tRNA. كان فرانسيس كريك اقترح ضرورة وجود نوع من جزيء مُحوِّل وسرعان ما تم تعريفه من قبل هولي، ساعد نيرنبرج وخورانا في تفسير هذه الصلة بين تسلسل نوكليوتيدات RNA المرسل وسلسلة الببتيد. في التجربة، قاما بتنقية tRNA من خلايا الخميرة ومنحا جائزة نوبل في عام 1968.[44]
1958: أوضحت تجربة ميسلسون ستال أن الحمض النووي يتم نسخه بشكل شبه متحفظ.[45]
1960: اكتشف جايكوب ومعاونيه «الاوبرون»، وهو مجموعة من الجينات التي تم تنسيقها من قبل المشغل «أوبراتور»[46][47]
1961: اكتشف فرانسيس كريك وسيدني برينر طفرات نقل الإطار. في التجربة، تم عزل الطفرات المستحثة بالبروفلافين من جينات بكتريا (T4 (rIIB . تسبب البروفلافين في إحداث الطفرات عن طريق إدراج نفسه بين قواعد الحمض النووي، مما يؤدي عادة إلى إدراج أو حذف زوج من قاعدة واحدة. الطفرة لا يمكن أن تنتج البروتين الوظيفي rIIB.[48] استُخدمت هذه الطفرات لإثبات أن ثلاث قواعد متسلسلة من الحمض النووي للجين rIIB تحدد كل حمض أميني صالح ناتج من شفرة البروتين . وبناء عليه فإن الشفرة الوراثية تتكون من رمز ثلاثي، حيث يحدد كل ثلاثي (يسمى كودون) حمض أميني معين.
1961: حدد كل من سيدني برينر، فرانسوا جاكوب وماثيو ميسلسون وظيفة RNA المرسِل.[49]
1961 - 1967: تضافرت جهود العلماء لفك الشفرة الوراثية، من ضمن هؤلاء مارشال نيرنبرج، هار غوبند خورانا، سيدني برينر وفرانسيس كريك.[50]
1964: أظهر هوارد تيمن باستخدام فيروسات RNA أن اتجاه الحمض النووي لنسخ الحمض النووي الريبي يمكن عكسه.
1964: نهاية الليسينكووية
1966: قام كل من مارشال جورج نيرنبرج، فيليب ليدر، هار غوبند خورانا بفك الشفرة الوراثية باستخدام تجارب مبلمر RNA المتجانس والمبلمر المغاير، والتي تمكنوا من خلالها من اكتشاف أي ثلاثة من الأحماض النووية الريبية تمت ترجمتها إلى أي من الأحماض الأمينية في خلايا الخميرة.
1969: التهجين الجزيئي للحمض النووي المشع إلى الحمض النووي ذو الإعداد الخلوي. بواسطة بارديو إم . إل وغال جي . جاي.
1970: تم اكتشاف إنزيمات القصر في دراسات البكتيريا، والمستدمية النزلية، على يد هاملتون سميث ودانيال ناتان، وهو ما مكن العلماء من قص ولصق الحمض النووي.[51]
1972: قام ستانلي كوهين نورمان وهربرت بوير في جامعة كاليفورنيا، سان فرانسيسكو، وجامعة ستانفورد ببناء الحمض النووي المؤتلف الذي يمكن تشكيله باستخدام اندونوكلياز القصر ليلتصق الحمض النووي بليغاز الحمض النووي لإعادة إلصاق «النهايات اللزجة» بالبلازميد البكتيري.[52]
عصر الجينوم
1972: كان والتر فايرس وفريقه في مختبر البيولوجيا الجزيئية بجامعة غنت (غنت، بلجيكا) أول من قام بتحديد تسلسل الجين: الجين المسئول عن البروتين المُغلف لجراثيم MS2.[53]
1976: قام والتر فايرس وفريقه بتحديد التسلسل الكامل لنوكليوتيدات الحمض النووي الريبي لجراثيم MS2.[54]
1976: إدخال جينات الخميرة في أي.كولاي للمرة الأولى .[55]
1977: توضيح تسلسل الحمض النووي لأول مرة من قبل فريد سانجر، ووالتر جيلبرت، وألان ماكسام حيث عمل كل منهم بشكل مستقل . حصل مختبر سانجر على تسلسل كامل للجينوم من الجراثيم Φ-X174.[56][57][58]
في أواخر العقد 1970: تم تطوير الأساليب غير المتناظرة لتمييز الحمض النووي. ساهمت التحسينات المتلاحقة في الكشف عن جزيئات المُراسل باستخدام الكيمياء المناعية وتقنية التألق المناعي، جنبا إلى جنب مع التقدم في المجهر الضوئي وتحليل الصور، مما جعل التقنية أكثر أمانا وسريعة وموثوق بها.
1980: طور كل من بول بيرغ ووالتر جيلبرت وفريدريك سانجر أساليب رسم بنية الحمض النووي. في عام 1972، تم إنتاج جزيئات الحمض النووي المؤتلف في مختبر بول بيرغ بجامعة ستانفورد . منح بيرغ جائزة نوبل في الكيمياء عام 1980 لبناء جزيئات الحمض النووي المؤتلف التي تحتوي على جينات فاج لمدا المدرجة في مول من DNA دائري صغير.[59]
1980: حصل ستانلي كوهين نورمان وهربرت بوير على أول براءة اختراع في الولايات المتحدة لاستنساخ الجينات، عن طريق إثبات نجاح استنساخ البلازميد وإدخال جينات غريبة في البكتيريا لإنتاج «بروتين غريب على كائن أحادي الخلية.» كان هذان العالمان قادرين على تكرار البروتينات مثل: هرمون النمو وإريثروبويتين والأنسولين. حصلت البراءة على نحو 300 مليون دولار في ترخيص حقوق الملكية لجامعة ستانفورد.[60]
1982: وافقت إدارة الغذاء والدواء الأمريكية (FDA) على إنتاج أول أنسولين بشري عن طريق الهندسة الوراثية، تمت مبدئيا الصناعة البيولوجية باستخدام طرق تهجين الحمض النووي بواسطة شركة جينينتيك في عام 1978.[61] بمجرد الموافقة عليها، نشطت عملية الاستنساخ لإنتاج كميات كبيرة من «هومولين» (بموجب ترخيص من قبل ايلي ليلي وشركاه).
1983: اخترع كاري بانكس موليس تفاعل البلمرة المتسلسل لتسهيل عمليه تضخيم الحمض النووي.[62]
1983: حصلت باربرا مكلينتوك على جائزة نوبل في الفسيولوجيا أو الطب لاكتشافها العناصر الوراثية المتنقلة. درست مكلينتوك الطفرات الناتجة عن الجينات القافزة، وكروموسوم التكسير في الذُرة ونشرت تقريرها الأول في عام 1948 عن الجين القافز أو الترانسبوزونات. وجدت أن الترانسبوزونات ملحوظة على نطاق واسع في الذُرة، رغم ذلك فإن أفكارها لم تتلق الاهتمام على نطاق واسع حتى 1960 و 1970 عندما تم اكتشاف الظاهرة نفسها في البكتيريا وذبابة الفاكهة.[63]
1985: أعلن أليك جيفريز عن طريقة بصمة الحمض النووي. جيفريز كان يدرس تباين الحمض النووي وتطور عائلات الجينات من أجل فهم الجينات المسببة للمرض.[64] في محاولة لتطوير عملية عزل العديد من الساتلايتس المصغرة (mini-satellites) في وقت واحد باستخدام المجسات الكيميائية، أخذ جيفريز أفلام الأشعة السينية للحمض النووي لفحصها ولاحظ أن مناطق الساتلايتس المصغرة تختلف اختلافا كبيرا من شخص إلى آخر. في تقنية بصمة الحمض النووي ، يتم هضم عينة الحمض النووي عن طريق معالجتها مع نوكلياز محدد أو نوكلياز حصر داخلي، ثم يتم فصل أجزائه كهربيا منتجا قالب متميز لكل نمط من النطاقات المنفردة للهلام.[65]
1986: اكتشف جيريمي ناتان الجينات المسئولة عن رؤية الألوان وعمى الألوان، وانضم للعمل مع ديفيد هوجنس ودوغلاس فولراث ورون ديفيس حيث كانوا يقومون بدراسة تعقيد شبكية العين.[66]
1989: اكتشف توماس تشيك أن RNA يمكنه أن يحفز التفاعلات الكيميائية،[67] وهو ما يعد أحد الاختراقات الأكثر أهمية في علم الوراثة الجزيئية، لأنه ألقي ضوءا على الوظيفة الحقيقية للقطاعات غير المفهومة من الحمض النووي.
1989: تم تحديد تسلسل الجين البشري الذي يشفر بروتين CFTR على يد فرانسيس كولينز ومختبر تشي تسوي. العيوب في هذا الجين تسبب التليف الكيسي.[68]
1992: كشف علماء أمريكيون وبريطانيون تقنية لاختبار الأجنة في المختبر (بزل) للبحث عن خلل وراثي مثل التليف الكيسي والهيموفيليا.
1993: حصل فيليب شارب وريتشارد روبرتس على جائزة نوبل لاكتشافهما أن الجينات في الحمض النووي تتكون من الإنترونات والإكسونات. وفقا لنتائجهما ليست كل النيوكليوتيدات الموجودة في شريط الحمض النووي الريبي RNA (الناتج عن نسخ DNA) يتم استخدامها في عملية الترجمة. ينقسم التسلسل الداخل في شريط الحمض النووي الريبي أولا بحيث لا يترك ورائه سوى جزء RNA بعد ترجمته إلى بولي ببتيد (بروتين).[69]
1994: اكتشاف أول جين مسبب لسرطان الثدي. BRCA الأول، تم اكتشافه من قبل الباحثين في مختبر كينج في جامعة كاليفورنيا في بيركلي في عام 1990، لكن تم استنساخه أول مرة في عام 1994. تم اكتشاف الجين الرئيسي الثاني ، BRCA الثاني المسبب لأعراض سرطان الثدي في وقت لاحق في عام 1994 من قبل البروفيسور مايكل ستراتون والدكتور ريتشارد ووستر.
1995: جينوم بكتيريا المستدمية النزلية، هو أول جينوم يتم تحديد تسلسله في الكائنات الحية الحرة.[70]
1996: خميرة الخباز، أحد أنواع الخميرة، هو أول تسلسل لجينوم من حقيقيات النواة يتم إصداره.
1996: اكتشف الكسندر ريتش Z-DNA، وهو نوع من الحمض النووي الذي يتواجد في حالة مؤقتة، حيث يظهر في بعض الحالات مصاحبًا لنسخ الحمض النووي.[71] الشكل Z-DNA من المرجح أن يحدث في مناطق من الحمض النووي الغنية بالسيتوزين والجوانين مع تركيزات عالية من الملح.[72]
1997: استنساخ النعجة دوللي بواسطة إيان ويلموت وزملاؤه من معهد روزلين في اسكتلندا.[73]
1998: تم إطلاق أول تسلسل جينوم لحقيقيات النواة متعددة الخلايا، الربداء الرشيقة.
2000: تم الانتهاء من تسلسل الجينوم الكامل لذبابة الفاكهة.
2001: انطلاق أول مشروع لتسلسل الجينوم البشري في وقت واحد من قبل «مشروع الجينوم البشري» وجينوم سيلير.
2003 (14 نيسان): الانتهاء بنجاح من مشروع الجينوم البشري مع 99٪ من تسلسل الجينوم وبدقة 99.99٪.[74]
2004: قدم ميرك لقاح لفيروس الورم الحليمي البشري الذي وعد بحماية المرأة من الإصابة بفيروس الورم الحليمي البشري 16 و 18، والذي يثبط نشاط الجينات المسببة للورم وتسبب معا 70٪ من حالات سرطان عنق الرحم.
2007: تتبع مايكل وروبي الأصول التطورية لفيروس نقص المناعة البشرية (HIV) عن طريق تحليل طفرات وراثية، والتي كشفت أن العدوى بفيروس نقص المناعة البشرية قد وقعت في الولايات المتحدة في وقت مبكر من العقد 1960.
2008: طورت هيوستون ـ بيزدـ انتروجين عقار أدفيكسين (في انتظار موافقة إدارة الغذاء والدواء العالمية)، باعتباره العلاج الجيني الأول لمرضى السرطان ومتلازمه لي-فراوميني، وذلك باستخدام نموذج من أدينوفيروس لتحمل ترميز الجين البديل للبروتين p53.
2016: تم تحديد تسلسل الجينوم في الفضاء الخارجي للمرة الأولى، مع رائدة فضاء وكالة ناسا كيت روبينز باستخدام جهاز MinION على متن محطة الفضاء الدولية.[75]
انظر أيضا
- دراسات كريسبر نتائج مشوشة من أبحاث الجينات القديمة
- تاريخ الفكر التطوري
- جينوم بشري
- مشروع الجينوم البشري
- قائمة الجينات البشرية
- غريغور يوهان مندل
- وليام باتسون
- توماس مورغان
- صفات معقدة (وراثة)
مراجع
- ^ Mayr, The Growth of Biological Thought, pp 635-640
- ^ Bhagwan، Bhagwan؛ Sharma، R.K. (1 يناير 2009). Charaka Samhita. Chowkhamba Sanskrit Series. ص. sharirasthanam II.26–27. ISBN:978-8170800125.
- ^ Zirkle، Conway (1941). "Natural Selection before the "Origin of Species"". Proceedings of the American Philosophical Society. ج. 84 ع. 1: 71–123. JSTOR:984852.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Cosman، Madeleine Pelner؛ Jones، Linda Gale. Handbook to life in the medieval world. Infobase Publishing. ص. 528–529. ISBN:0-8160-4887-8.
- ^ HaLevi, Judah, translated and annotated by N. Daniel Korobkin. The Kuzari: In Defense of the Despised Faith, p. 38, I:95: "This phenomenon is common in genetics as well—often we find a son who does not resemble his father at all, but closely resembles his grandfather. Undoubtedly, the genetics and resemblance were dormant within the father even though they were not outwardly apparent. Hebrew by Ibn Tibon, p.375: ונראה כזה בענין הטבעי, כי כמה יש מבני האדם שאינו דומה לאב כלל אך הוא דומה לאבי אביו ואין ספק כי הטבע ההוא והדמיון ההוא היה צפון באב ואף על פי שלא נראה להרגשה
- ^ Mayr, The Growth of Biological Thought, pp 640-649
- ^ Mayr, The Growth of Biological Thought, pp 649-651
- ^ سيدهارتا موكرجي (2016) The Gene:An intimate history Chapter 4.
- ^ أ ب سيدهارتا موكرجي (2016) The Gene:An intimate history Chapter 5.
- ^ Gerstein MB، Bruce C، Rozowsky JS، Zheng D، Du J، Korbel JO، Emanuelsson O، Zhang ZD، Weissman S، Snyder M (يونيو 2007). "What is a gene, post-ENCODE? History and updated definition". Genome Research. ج. 17 ع. 6: 669–681. DOI:10.1101/gr.6339607. PMID:17567988.
- ^ Steinman RM، Moberg CL (فبراير 1994). "A triple tribute to the experiment that transformed biology". The Journal of Experimental Medicine. ج. 179 ع. 2: 379–84. DOI:10.1084/jem.179.2.379. PMC:2191359. PMID:8294854.
- ^ Min Jou W، Haegeman G، Ysebaert M، Fiers W (مايو 1972). "Nucleotide sequence of the gene coding for the bacteriophage MS2 coat protein". Nature. ج. 237 ع. 5350: 82–8. Bibcode:1972Natur.237...82J. DOI:10.1038/237082a0. PMID:4555447.
- ^ Pearson H (مايو 2006). "Genetics: what is a gene?". Nature. ج. 441 ع. 7092: 398–401. Bibcode:2006Natur.441..398P. DOI:10.1038/441398a. PMID:16724031.
- ^ Pennisi E (يونيو 2007). "Genomics. DNA study forces rethink of what it means to be a gene". Science. ج. 316 ع. 5831: 1556–1557. DOI:10.1126/science.316.5831.1556. PMID:17569836.
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. pp.210
- ^ Vries, H. de (1889) Intracellular Pangenesis [1] ("pan-gene" definition on page 7 and 40 of this 1910 translation in English) نسخة محفوظة 25 يوليو 2018 على موقع واي باك مشين.
- ^ Principles of Biochemistry / Nelson and Cox – 2005. pp.681
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. pp.383-384
- ^ Cell and Molecular Biology, Concepts and experiments / Gerald Karp –5th Ed (2008). pp. 430-431
- ^ Ernest W. Crow؛ James F. Crow (1 يناير 2002). "100 years ago: Walter Sutton and the chromosome theory of heredity". Genetics. ج. 160 ع. 1: 1–4. PMC:1461948. PMID:11805039. مؤرشف من الأصل في 2011-01-01.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|last-author-amp=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ O'Connor, C. & Miko, I. (2008) Developing the chromosome theory. Nature Education [2] نسخة محفوظة 11 أغسطس 2017 على موقع واي باك مشين.
- ^ Sutton, W. S. (1902) On the morphology of the chromosome group in Brachystola magna. Biological Bulletin 4:24-3, pp. 39 [3] نسخة محفوظة 01 سبتمبر 2006 على موقع واي باك مشين.
- ^ Online copy of William Bateson's letter to Adam Sedgwick نسخة محفوظة 29 أبريل 2014 على موقع واي باك مشين.
- ^ Bateson, William (1907). "The Progress of Genetic Research". في Wilks, W. (editor) (المحرر). Report of the Third 1906 International Conference on Genetics: Hybridization (the cross-breeding of genera or species), the cross-breeding of varieties, and general plant breeding. London: Royal Horticultural Society.
{{استشهاد بمنشورات مؤتمر}}:|محرر=باسم عام (مساعدة)- Although the conference was titled "International Conference on Hybridisation and Plant Breeding", Wilks changed the title for publication as a result of Bateson's speech.
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. p.99
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. pp.147
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. pp.109
- ^ Online summary of "Real Genetic vs. Lysenko Controversy نسخة محفوظة 19 يناير 2017 على موقع واي باك مشين.
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. pp.190
- ^ Beadle GW, Tatum EL. Genetic Control of Biochemical Reactions in Neurospora. Proc Natl Acad Sci U S A. 1941 Nov 15;27(11):499-506. ببمد: 16588492
- ^ Luria، SE؛ Delbrück، M (نوفمبر 1943). "Mutations of Bacteria from Virus Sensitivity to Virus Resistance". Genetics. ج. 28: 491–511. PMC:1209226. PMID:17247100.
- ^ Oswald T. Avery؛ Colin M. MacLeod؛ Maclyn McCarty (1944). "Studies on the chemical nature of the substance inducing transformation of pneumococcal types: Induction of transformation by a desoxyribonucleic acid fraction isolated from pneumococcus type III". Journal of Experimental Medicine. ج. 79 ع. 1: 137–58. DOI:10.1084/jem.79.2.137. PMC:2135445. PMID:19871359.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|last-author-amp=تم تجاهله يقترح استخدام|name-list-style=(مساعدة)35th anniversary reprint available - ^ Luria SE. Reactivation of Irradiated Bacteriophage by Transfer of Self-Reproducing Units. Proc Natl Acad Sci U S A. 1947 Sep;33(9):253-64. ببمد: 16588748
- ^ Bernstein C. Deoxyribonucleic acid repair in bacteriophage. Microbiol Rev. 1981 Mar;45(1):72-98. Review. ببمد: 6261109
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. pp.217 Table 9.1
- ^ Tamm، C.؛ Herman، T.؛ Shapiro، S.؛ Lipschitz، R.؛ Chargaff، E. (1953). "Distribution Density of Nucleotides within a Desoxyribonucleic Acid Chain". Journal of Biological Chemistry. ج. 203 ع. 2: 673–688. مؤرشف من الأصل في 2017-07-19.
- ^ HERSHEY AD, CHASE M. Independent functions of viral protein and nucleic acid in growth of bacteriophage. J Gen Physiol. 1952 May;36(1):39-56. ببمد: 12981234
- ^ "Due credit". Nature. ج. 496: 270. 18 أبريل 2013. DOI:10.1038/496270a. مؤرشف من الأصل في 2019-04-30.
- ^ Watson، JD؛ Crick، FH (أبريل 1953). "Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid". Nature. ج. 171 ع. 4356: 737–8. Bibcode:1953Natur.171..737W. DOI:10.1038/171737a0. PMID:13054692.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Todd، AR (1954). "CHEMICAL STRUCTURE OF THE NUCLEIC ACIDS" (PDF). Proc. Natl. Acad. Sci. U.S.A. ج. 40: 748–55. PMC:534157. PMID:16589553. مؤرشف من الأصل (PDF) في 2019-12-19.
- ^ Wright, Pearce (11 ديسمبر 2001). "Joe Hin Tjio The man who cracked the chromosome count". The Guardian. مؤرشف من الأصل في 2017-08-25.
- ^ Cell and Molecular Biology, Concepts and experiments / Gerald Karp –5th Ed (2008) pp. 548
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. (Discovery of DNA polymerase I in E. Coli) pp.255
- ^ Cell and Molecular Biology, Concepts and experiments / Gerald Karp –5th Ed (2008) pp. 467-469
- ^ Meselson M, Stahl FW. THE REPLICATION OF DNA IN ESCHERICHIA COLI. Proc Natl Acad Sci U S A. 1958 Jul 15;44(7):671-82. ببمد: 16590258
- ^ Jacob F1, Perrin D, Sánchez C, Monod J, Edelstein S. [The operon: a group of genes with expression coordinated by an operator. C.R.Acad. Sci. Paris 250 (1960) 1727-1729]. [Article in English, French] C R Biol. 2005 Jun;328(6):514-20. ببمد: 15999435
- ^ JACOB F, PERRIN D, SANCHEZ C, MONOD J. [Operon: a group of genes with the expression coordinated by an operator]. C R Hebd Seances Acad Sci. 1960 Feb 29;250:1727-9. French. ببمد: 14406329
- ^ Crick، FH؛ Barnett، L؛ Brenner، S؛ Watts-Tobin، RJ (1961). "General nature of the genetic code for proteins". Nature. ج. 192: 1227–32. DOI:10.1038/1921227a0. PMID:13882203.
- ^ Molecular Station: Structure of protein coding mRNA (2007) نسخة محفوظة 03 أبريل 2012 على موقع واي باك مشين. [وصلة مكسورة]
- ^ CRICK FH, BARNETT L, BRENNER S, WATTS-TOBIN RJ. General nature of the genetic code for proteins. Nature. 1961 Dec 30;192:1227-32. ببمد: 13882203
- ^ Principles of Genetics / D. Peter Snustad, Michael J. Simmons – 5th Ed. (Discovery of DNA polymerase I in E. Coli) pp.420
- ^ Genetics and Genomics Timeline: The discovery of messenger RNA (mRNA) by Sydney Brenner, Francis Crick, Francois Jacob and Jacques Monod [4] نسخة محفوظة 22 ديسمبر 2017 على موقع واي باك مشين.
- ^ Min Jou، W؛ Haegeman، G؛ Ysebaert، M؛ Fiers، W. (مايو 1972). "Nucleotide sequence of the gene coding for the bacteriophage MS2 coat protein". Nature. ج. 237 ع. 5350: 82–8. Bibcode:1972Natur.237...82J. DOI:10.1038/237082a0. PMID:4555447.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Fiers، W؛ Contreras، R؛ Duerinck، F؛ Haegeman، G؛ Iserentant، D؛ Merregaert، J؛ Min Jou، W؛ Molemans، F؛ وآخرون (1976). "Complete nucleotide-sequence of bacteriophage MS2-RNA - primary and secondary structure of replicase gene". Nature. ج. 260 ع. 5551: 500–507. Bibcode:1976Natur.260..500F. DOI:10.1038/260500a0. PMID:1264203.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Genetics, The hisB463 Mutation and Expression of a Eukaryotic Protein in Escherichia coli Vol. 180, 709-714, October 2008 [5] نسخة محفوظة 14 سبتمبر 2009 على موقع واي باك مشين.
- ^ Sanger، F؛ Air، GM؛ Barrell، BG؛ Brown، NL؛ Coulson، AR؛ Fiddes، CA؛ Hutchison، CA؛ Slocombe، PM؛ Smith، M.؛ وآخرون (فبراير 1977). "Nucleotide sequence of bacteriophage phi X174 DNA". Nature. ج. 265 ع. 5596: 687–95. Bibcode:1977Natur.265..687S. DOI:10.1038/265687a0. PMID:870828.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Sanger، F؛ Nicklen، S؛ Coulson، AR (ديسمبر 1977). "DNA sequencing with chain-terminating inhibitors" (PDF). Proc. Natl. Acad. Sci. U.S.A. ج. 74: 5463–7. DOI:10.1073/pnas.74.12.5463. PMC:431765. PMID:271968. مؤرشف من الأصل (PDF) في 2019-12-19.
- ^ Principles of Biochemistry / Nelson and Cox – 2005. pp.296-298
- ^ Cell and Molecular Biology, Concepts and experiments / Gerald Karp –5th Ed (2008). pp. 976 - 977
- ^ Patents 4 Life: Bertram Rowland 1930–2010. Biotech Patent Pioneer Dies (2010) [6] نسخة محفوظة 21 أبريل 2019 على موقع واي باك مشين.
- ^ Funding Universe: Genentech, Inc نسخة محفوظة 04 مارس 2012 على موقع واي باك مشين.
- ^ Cell and Molecular Biology, Concepts and experiments / Gerald Karp –5th Ed (2008). Pp. 763
- ^ The Significance of Responses of the Genome to Challenge / Barbara McClintock – Science New Series, Vol. 226, No. 4676 (1984), pp. 792-801
- ^ Lemelson MIT Program—Inventor of the week: Alec Jeffreys – DNA FINGERPRINTING (2005) [7] نسخة محفوظة 01 مارس 2014 على موقع واي باك مشين.
- ^ Jeffreys، AJ؛ Wilson، V؛ Thein، SL (1985). "Individual-specific 'fingerprints' of human DNA". Nature. ج. 316: 76–79. DOI:10.1038/316076a0. PMID:2989708.
- ^ Wikidoc: Color Blindness – Inheritance pattern of Color Blindness (2010) [8] نسخة محفوظة 14 سبتمبر 2016 على موقع واي باك مشين.
- ^ Cell and Molecular Biology, Concepts and experiments / Gerald Karp –5th Ed (2008) pp. 478
- ^ Kerem B؛ Rommens JM؛ Buchanan JA؛ Markiewicz؛ Cox؛ Chakravarti؛ Buchwald؛ Tsui (سبتمبر 1989). "Identification of the cystic fibrosis gene: genetic analysis". Science. ج. 245 ع. 4922: 1073–80. Bibcode:1989Sci...245.1073K. DOI:10.1126/science.2570460. PMID:2570460. مؤرشف من الأصل في 2020-03-26.
- ^ A Century of Nobel Prize Recipients / Francis Leroy - 2003. pp 345
- ^ Fleischmann RD؛ Adams MD؛ White O؛ Clayton؛ Kirkness؛ Kerlavage؛ Bult؛ Tomb؛ Dougherty؛ Merrick؛ McKenney؛ Sutton؛ Fitzhugh؛ Fields؛ Gocyne؛ Scott؛ Shirley؛ Liu؛ Glodek؛ Kelley؛ Weidman؛ Phillips؛ Spriggs؛ Hedblom؛ Cotton؛ Utterback؛ Hanna؛ Nguyen؛ Saudek؛ وآخرون (يوليو 1995). "Whole-genome random sequencing and assembly of Haemophilus influenzae Rd". Science. ج. 269 ع. 5223: 496–512. Bibcode:1995Sci...269..496F. DOI:10.1126/science.7542800. PMID:7542800. مؤرشف من الأصل في 2020-03-26.
- ^ Rich، A؛ Zhang، S (يوليو 2003). "Timeline: Z-DNA: the long road to biological function" (PDF). Nature Reviews Genetics. ج. 4: 566–572. DOI:10.1038/nrg1115. PMID:12838348. مؤرشف من الأصل (PDF) في 2017-08-30.
- ^ "The Discovery of Z-DNA: the Work of Alexander Rich". The Journal of Biological Chemistry. ج. 284 ع. 51: e23–e25. PMC:2791029.
- ^ CNN Interactive: A sheep cloning how-to, more or less(1997) http://www.cnn.com/TECH/9702/24/cloning.explainer/index.html نسخة محفوظة 31 أكتوبر 2020 على موقع واي باك مشين.
- ^ National Human Genome Research Institute / The Human Genome Project Completion: FAQs (2010) [9] نسخة محفوظة 11 ديسمبر 2017 على موقع واي باك مشين.
- ^ "DNA sequenced in space for first time". BBC News. 30 أغسطس 2016. مؤرشف من الأصل في 2019-04-22. اطلع عليه بتاريخ 2016-08-31.
وصلات خارجية
- Olby's "Mendel, Mendelism, and Genetics," at MendelWeb
- ""Experiments in Plant Hybridization" (1866), by Johann Gregor Mendel," by A. Andrei at the Embryo Project Encyclopedia
- http://www.accessexcellence.org/AE/AEPC/WWC/1994/geneticstln.html
- http://www.sysbioeng.com/index/cta94-11s.jpg
- http://www.esp.org/books/sturt/history/
- http://cogweb.ucla.edu/ep/DNA_history.html
- http://news.bbc.co.uk/1/hi/in_depth/sci_tech/2000/human_genome/749026.stm
- http://www.hchs.hunter.cuny.edu/wiki/index.php?title=Modern_Science&printable=yes
- http://jem.rupress.org/content/79/2/137.full.pdf
- http://www.nature.com/physics/looking-back/crick/Crick_Watson.pdf
- Todd، AR (1954). "CHEMICAL STRUCTURE OF THE NUCLEIC ACIDS" (PDF). Proc. Natl. Acad. Sci. U.S.A. ج. 40: 748–55. PMC:534157. PMID:16589553. مؤرشف من الأصل (PDF) في 2019-12-19.
- http://www.genomenewsnetwork.org/resources/timeline/1960_mRNA.php
- http://www.molecularstation.com/molecular-biology-images/data/503/MRNA-structure.png
- http://www.genomenewsnetwork.org/resources/timeline/1973_Boyer.php
- http://www.genetics.org/cgi/content/full/180/2/709
- Sanger، F؛ Nicklen، S؛ Coulson، AR (ديسمبر 1977). "DNA sequencing with chain-terminating inhibitors" (PDF). Proc. Natl. Acad. Sci. U.S.A. ج. 74: 5463–7. DOI:10.1073/pnas.74.12.5463. PMC:431765. PMID:271968. مؤرشف من الأصل (PDF) في 2019-12-19.
- Jeffreys، AJ؛ Wilson، V؛ Thein، SL (1985). "Individual-specific 'fingerprints' of human DNA". Nature. ج. 316: 76–79. DOI:10.1038/316076a0. PMID:2989708. مؤرشف من الأصل في 2017-06-06.
- "Biological Catalysis by RNA". Annual Review of Biochemistry. ج. 55: 599–629. DOI:10.1146/annurev.bi.55.070186.003123. مؤرشف من الأصل في 2020-01-13.
- http://www.cnn.com/TECH/9702/24/cloning.explainer/index.html
- http://www.genome.gov/11006943
| في كومنز صور وملفات عن: تاريخ علم الجينات |

