|
تضامنًا مع حق الشعب الفلسطيني |
التهاب الأمعاء بالفيروس العجلي
| التهاب الأمعاء بالفيروس العجلي | |
|---|---|
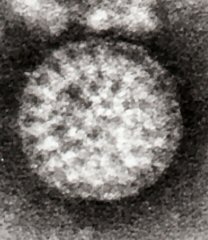
الفيروس العجلي A من براز طفل مصاب.
| |
| تعديل مصدري - تعديل |
التهاب اللأمعاء بالفيروس العجلي هو المسبب الأكثر انتشارّا للإسهال الحاد لدى الأطفال.[1] هذا المرض ناتج عن الفيروس العجلي، وهو جنس من فيروس RNA المزدوج في فصيلة الفيروسات التنفسية المعوية اليتيمة. بحلول سن الخامسة تقريبًا جميع الأطفال في العالم يكونون قد أصيبوا بالفيروس العجلي مرة واحدة على الأقل.[2] ولكن مع كل عدوى، تتطور المناعة، وتقل حدة الإصابات اللاحقة؛ ونادرّا ما يتأثر البالغون.[3] هناك خمسةأنواع من هذا الفيروس، يشار إليهم بـ A، B، C، D، و E.[4] الفيروس العجلي A، هو الأكثر انتشارًا، وهو المسبب لأكثر من 90% من الإصابات لدى البشر.
هذا الفيروس ينتقل عبر الطريق الفموي-الشرجي. ويصيب ويضر الخلايا التي تغطي الأمعاء الدقيقة ويسببالتهابًا معديًا معويًا (والذي يسمى أحيانًا «إنفلونزا المعدة» على الرغم من عدم وجود أي علاقة بينه وبين الإنفلونزا). على الرغم من اكتشاف الفيروس العجلي في 1973 ومساهمته في إدخال 50% من الأطفال الرضع والأطفال الصغار للمستشفى بسبب الإسهال الشديد،[5] إلا أن أهميته لا تزال غير معروفة على نحو واسع لدى مجتمع الصحة العامة ولا سيما في الدول النامية.[6] بالإضافة إلى تأثيرها على صحة الإنسان، الفيروسات العجلية تصيب الحيوانات أيضًا، وهي عامل ممرض لدى الماشية.[7]
الفيروس العجلي مرض أطفال يمكن التحكم به غالبًا بسهولة، لكن لايزال تقريبًا 500,000 طفل حول العالم تحت سن الخامسة يموتون بسبب عدوى الفيروس العجلي سنويًا[8] ويمرض ما يقارب المليونين بشدة.[6] في الولايات المتحدة الأمريكية، قبل الشروع ببرنامج تطعيم الفيروس العجلي، تسبب هذا الفيروس بنحو 2.7 مليون حالة التهاب معدي معوي شديد لدى الأطفال، وإدخال ما يقارب 60,000 حالة للمستشفى، وحوالي 37 حالة وفاة سنويًا.[9] تركز حملات الصحة العامة لمكافحة الفيروس العجلي على توفير العلاج بالإمهاء الفموي للأطفال المصابين والتطعيم لمنع هذا المرض.[10] انخفضت معدلات حدوث وشدة عدوى الفيروس العجلي في الدول التي أضافت لقاح الفيروس العجلي إلى سياسات تطعيم الأطفال الروتينية لديها.[11]
الأعراض
التهاب المعدة والأمعاء الناتج عن الفيروس العجلي مرض خفيف أو شديد بالتقيؤ والإسهال المائي، والحمى المنخفضة. عندما يصاب الطفل بهذا الفيروس، تكون مدة فترة الحضانة يومان تقريبًا قبل ظهور الأعراض.[12] غالبًا ما تبدأ الأعراض بالتقيؤ ويليها أربع إلى ثمانية أيام من الإسهال الغزير. تجفاف شائع بكثرة عند الإصابة بالفيروس العجلي أكثر من شيوعه لدى مسببات الأمراض البكتيرية، وهو المسبب الأكثر شيوعًا لحالات الوفاة ذات الصلة بالفيروس العجلي.[13]
يمكن أن تحدث عدوى الفيروس العجلي A في جميع مراحل الحياة، لكن الأولى غالبًا هي التي تنتج أعراضًا، أما الإصابات اللاحقة عادة ما تكون خفيفة أو عديمة الأعراض،[14][15] حيث أن الجهاز المناعي يوفر بعض الحماية.[16][17] وبالتالي، معدل الإصابات التي تنتج أعراض هي أعلى لدى الأطفال تحت السنتين من العمر وتنخفض بشكل تدريجي عند بلوغ 45 عامَا.[18] الإصابات لدى الأطفال حديثي الولادة -على الرغم من شيوعها- إلا أنها عادة ما تكون خفيفة الأعراض أو عديمتها؛ الأعراض الأكثر حدة عادة ما تحدث لدى الأطفال من سن الستة شهور وحتى السنتين من العمر، الكبار بالسن، والأشخاص الذين يعانون من نقص المناعة. بسبب المناعة المكتسبة في الطفولة، معظم البالغين غير معرضين للإصابة بالفيروس العجلي؛ والالتهاب المعدي المعوي لدى البالغين عادة ما يكون له مسبب آخر غير الفيروس العجلي، ولكن الإصابات عديمة الأعراض لدى البالغين قد تحافظ على انتشار العدوى لدى المجتمع.[19]
الفيرولوجيا

الانتقال
ينتقل الفيروس العجلي عن الطريق الفموي-الشرجي، من خلال لمس الأيدي، والأسطح، والأجسام الملوثة،[20] وقد ينتقل أيضًا بالطريق التنفسي.[1] قد يحتوي براز الشخص المصاب على أكثر من 10 تريليونات جسم معدي لكل جرام؛ أقل من 100 من هذه الأجسام مطلوب لنقل العدوى لشخص أخر.[3]
الفيروسات العجلية مستقرة في البيئة، إذ وُجدت في عينات من مصبات الأنهار بمستويات مرتفعة تصل إلى 1-5 جسيمات معدية لكل جالون أمريكي.[21] التدابير الصحية المناسبة للقضاء على البكتيريا والطفيليات تبدو غير فعالة للسيطرة على الفيروس العجلي، إذ تتشابه حالات العدوى لدى الدول ذات المعايير العالية والمنخفضة.
الأنواع
هناك خمسة أصناف من الفيروس العجلي، يشار إليها بـ A، B، C، D، وE. أكثر ما يصيب البشر الأصناف A، B، C، ولكن الصنف الأكثر شيوعًا هو A. الأصناف الخمسة جميعها تسبب المرض لدى الحيوانات الأخرى.[22] توجد سلالات مختلفة في الفيروس العجلي A، تسمى أنماط مصلية.[23] يُستَخدم نظام تصنيف مزدوج كالذي يستخدم مع فيروس الإنفلونزا، وذلك استنادًا إلى نوعين من البروتين على سطح الفيروس. البروتين السكري VP7 يحدد الأنماط المصلية G، أما البروتين الحساس للبيبتيداز VP4 فيحدد الأنماط المصلية P.[24] وبسبب كون الجينين الذين يحددان أنماط-G وأنماط-P قابلين للانتقال بشكل منفصل إلى الفيروسات الذرية، وجدت تراكيب مختلفة.[25]
التنسُّخ
أكثر ما يكون تنسُّخ الفيروس العجلي في القناة الهضمية،[26] ويصيب الخلايا المعوية في الزغابة المعوية للأمعاء الدقيقة، مما يؤدي إلى تغيرات هيكلية ووظيفية للأنسجة الطلائية.[27] يزيد الغشاء البروتيني الثلاثي من مقاومة الفيروس لدرجة حموضة المعدة والأنزيمات الهاضمة في القناة الهضمية.
يدخل الفيروس إلى الخلايا عن طريق الإلتقام المتواسط بالمستقبلات ويكوّن حويصلات تعرف بالجسيمات الداخلية. البروتينات التي على الطبقة الثالثة (مرتفعات VP7 VP4) تمزّق غشاء الجسيمات الداخلية، مما يُسبّب اختلافًا في تركيز الكالسيوم. وهذا يسبب تعطيل مثاليث VP7 إلى وحيدات بروتين مفردة، تاركًا طبقتي البروتين VP2 وVP6 حول الدنا الفيروسي المزدوج، ليشكلا جسيمًا ثنائي الطبقة (DLP).[28]
أشرطة الدنا المزدوجة الإحدي عشر تبقى تحت حماية قشرتي البروتين، وببقائها في اللُب، يتجنب RNA الفيروس ردات الفعل الفطرية لمناعة المضيف المسماة تداخل الحمض النووي الريبوزي التي تثار بوجود RNA المزدوج.
في غضون فترة العدوى، ينتج الفيروس العجلي مرسال الحمض النووي الريبوزي لتخليق البروتين وتكرار الجين. معظم بروتينات الفيروس العجلي تتراكم في الجبلة الفيروسية، حيث يتكرر الحمض النووي الريبوزي (RNA) وتجمع الجسيمات ثنائية الطبقة. تتشكل الجبلة الفيروسية حول نواة الخلية بشكل مبكر قد يصل إلى ساعتين من الإصابة بالفيروس، وتتألف من مصانع فيروسية يعتقد بأنها مصنوعة من بروتينين فيروسيين غير هيكليين: NSP5 وNSP2. كبح NSP5 بواسطة تداخل الحمض النووي الريبوزي يتسبب بانخفاض حاد في تكرار الفيروس العجلي. ترحل الجسيمات ثنائية الطبقة إلى الشبكة الإندوبلازمية حيث تكتسب طبقتها الخارجية الثالثة، (المكونة من VP7 وVP4). وتتحرر الفيروسات الذرية من الخلية بالانحلال.[29][30][31]
الفيزيولوجيا المرضية

ينجم الإسهال عن عدة أنشطة للفيروس. يحدث سوء الامتصاص بسبب تدمير خلايا القناة الهضمية التي تسمى ب«الخلايا المعوية». يحث بروتين الفيروس العجلي السام معويًا NSP4 إفراز الكلوريد بحسب السن وأيون الكالسيوم، ويعطل إعادة امتصاص الماء المتواسط بناقل SGLT1، ويقلل كما يبدو من نشاط أنزيمات دي سكاريداز المتواجدة في غشاء الحافة الفرشاتية، وربما ينشط الإفراز اللاإردي للكالسيوم المعتمد على الأيون في الجهاز العصبي المعوي.[32] تفرز الخلايا المعوية الصحية أنزيم اللكتاز في الأمعاء الدقيقة؛ الحساسية المفرطة للحليب الناتجة عن نقص اللكتاز هي أحد أعراض الإصابة بالفيروس العجلي،[33] والتي قد تستمر لعدة أسابيع.[34] يعود إسهال خفيف عند إعادة الحليب إلى النظام الغذائي للطفل، بسبب التخمر البكتيري للاكتوز ثنائي السكر في القناة الهاضمة.[35]
التشخيص
تشخيص عدوى الفيروس العجلي غالبًا ما تتبع التشخيص بالتهاب معدي معوي كسبب للإسهال الشديد. أغلب الأطفال الذين يدخلون المستشفى بالتهاب معدي معوي يتم اختبارهم للفيروس العجلي A.[36][37] يتم القيام بتشخيص دقيق للإصابة بالفيروس العجلي A باكتشاف الفيروس في براز الطفل عن طريق المقايسة المناعية المرتبطة بالإنزيم (إليزا). توجد عدة أدوات اختبار مرخصة حساسة ونوعيّة تكشف جميع الأنماط المصلية للفيروس العجلي A.[38] تستعمل طرق أخرى، كالمجهر الإلكتروني وتفاعل البوليميراز المتسلسل، في المختبرات البحثية.[39] النسخ العكسي لتفاعل البوليميراز المتسلسل (تفاعل البوليميراز المتسلسل) يستطيع أن يكشف ويحدد جميع الأصناف والأنماط المصلبة للفيروس العجلي البشري.[40]
الوقاية
تحسين التصريف الصحّي لا يُقلل من انتشار أمراض الفيروسات العجلية، ومعدل الدخول للمستشفى يظل عاليًا على الرغم من استعمال أدوية الإمهاء الفموي. أهم تدخل صحي عام هو التطعيم.[2] يوجد لقاحين للفيروس العجلي ضد الإصابة بالفيروس العجلي A آمنين وفعالين لدى الأطفال:[41] هما روتاريكس (Rotarix) أنتجته شركة غلاكسو سميث كلاين[42] وروتاتيك (RotaTeq) أنتجته شركة ميرك.[43] وكلا اللقاحين يؤخذان فمويًا ويحتويان على فيروس حي مُضعّف.[41]
لقاحات الفيروس العجلي مرخصة في أكثر من 100 دولة، ولكن 17 دولة فقط قدمت تطعيمات روتينية للفيروس العجلي.[44] بعد إدخال التطعيم الروتيني للفيروس العجلي في الولايات المتحدة الأمريكية في 2006، انخفض العبء الصحي للالتهاب المعدي المعوي الناتج عن الفيروس العجلي بشكل كبير وسريع على الرغم من انخفاض معدلات التغطية مقارنة بالتطعيمات الروتينية الأخرى للرضع.[45] التجارب الإكلينيكية للقاح الفيروس العجلي روتاريكس (Rotarix) في أفريقيا الجنوبية وملاوي وجدت أن اللقاح قلل بشكل كبير نوبات الإسهال الحاد التي يسببها الفيروس العجلي، وصار ممكنا الوقاية من العدوى بالتطعيم.[46] مراجعة لمؤسسة كوكرين في 2012 ل41 تجربة إكلينيكية تضمنت 186,263 مشاركًا استنتجت بأن روتاريكس (Rotarix) وروتاتيك (RotaTeq) لقاحين فعالين.[47] توجد لقاحات أخرى للفيروس العجلي تحت التطوير.[48] منظمة الصحة العالمية (WHO) توصي بإدخال تطعيمات الفيروس العجلي في جميع برامج التمنيع الوطنية.[49] هبط حدوث إصابات الفيروس العجلي وحدّتها بشكل كبير لدى الدول التي نفّذت هذه التوصية.[11][41]
برنامج تطعيم الفيروس العجلي هو تعاون بين برنامج التكنولوجيا الملائمة في مجال الصحة (PATH)، ومنظمة الصحة العالمية (WHO)، ومركز مكافحة الأمراض واتقائها الأمريكي. هذا البرنامج يهدف إلى خفض معدل مرض ووفيات الأطفال من أمراض الإسهال عبر إتاحة لقاح ضد الفيروس العجلي في البلدان النامية.[50]
العلاج والتشخيص
علاج عدوى الفيروس العجلي المكتسبة غير محدد ويتضمن التحكم بالأعراض، والأهم، المحافظة على التميه.[10] إذا لم يعالج الفيروس فقد يموت الأطفال المصابون بسبب شدة الجفاف الناتجة عنه.[51] اعتمادًا على شدة الإسهال، يتضمن العلاج الإمهاء الفموي، وخلال ذلك يعطى الطفل كمية مياه زائدة تحتوي على كميات قليلة من الملح والسكر.[52] بعض الإصابات تكون خطيرة لدرجة تستدعي التنويم في المستشفى حيث تعطى السوائل بالتستيل الوريدي أو عن طريق الأنبوب الأنفي المعدي، وتتم المحافظة على كهارل الدم وسكرياته.[53] المضادات الحيوية لا يوصى بها.
من النادر أن تسبب عدوى الفيروس العجلي مضاعفات أخرى وبالنسبة للطفل المعالج بشكل جيد يكون مآله ممتازًا.[54]
علم الأوبئة

الفيروس العجلي A، والذي يمثل 90% من حالات التهاب المعدة والأمعاء لدى البشر،[55] هو مرض متوطن في جميع أنحاء العالم. يسبب الفيروس العجلي سنويًا ملايين حالات الإسهال في الدول النامية، مليوني حالة تقريبًا تؤدي إلى دخول المستشفى[6] وما يقدر ب453,000 حالة تسبب موت الطفل في عمر يقل عن 5 سنوات.[8] ترتبط 40% من حالات التنويم في المستشفيات بالإسهال لدى الأطفال الأصغر من 5 سنوات على مستوى العالم.[56]
في الولايات المتحدة الأمريكية وحدها—قبل انطلاق مشروع تطعيم الفيروس العجلي[57]—كانت تحدث أكثر من 2.7 مليون حالة لالتهاب المعدة والأمعاء بالفيروس العجلي سنويا، 60,000 أدخلوا المستشفى و37 ماتوا نتيجة لإصابتهم بهذا الفيروس.[9] الدور الرئيس الذي يلعبه الفيروس العجلي في الإسهال غير معترف به إلى حد واسع في مجتمع الصحة العامة[58] خاصةً في الدول النامية.[6] تقريبًا جميع الأطفال قد أصيبوا بالفيروس العجلي بحلول سن الخامسة.[59] هذا الفيروس هو السبب الرئيسي الوحيد للإسهال الحاد لدى الأطفال والأطفال الرضع، كونه مسؤولًا عن 20% من الحالات، ولتمثيله 50% من الحالات التي تتطلب الدخول إلى المستشفى.[6] الفيروس العجلي يسبب 37% من الوفيات الناتجة عن الإسهال و5% من جميع الوفيات للأطفال دون سن الخامسة. نسبة دخول الذكور إلى المستشفى أعلى بمرتين من الإناث.[5][60] أكثر وقت للإصابة بالفيروس العجلي في موسم البرد الجاف.[61] العدد الناتج عن الطعام الملوث غير معروف.[62]
تفشي إسهال الفيروس العجلي A شائع لدى الأطفال الرضع نزلاء المستشفيات، والأطفال الصغار الذين يذهبون إلى الحضانة، وكبار السن في دور العجائز.[63] حدث تفشٍّ للفيروس عن طريق المياه المحلية الملوثة في كولورادو في 1981.[64] أثناء 2005، حدث أكبر وباء مسجل للإسهال في نيكاراغوا. تفشي هذا المرض الحاد والغير معتاد كان مرتبطًا بطفرات جينية في جينوم الفيروس العجلي A، لعلها ساهمت في نجاة الفيروس من المناعة السائدة لدى السكان.[65] تفشٍّ آخر لهذا المرض حدث أيضًا في البرازيل في1977.[66]
الفيروس العجلي B، والذي يدعى أيضًا فيروس إسهال البالغين العجلي أو ADRV، سببّ وباءًا كبيرًا للإسهال الحاد وأصاب آلاف الأشخاص من جميع الأعمار في الصين. هذه الأوبئة حدثت كنتيجة لتلوث مياه الشرب بمياه الصرف الصحي.[67][68] عداوى الفيروس العجلي B حدثت أيضًا في الهند في 1998؛ والسلالة المسببة كانت تسمى CAL على خلاف ADRV، سلالة CAL هي سلالة مستوطنة.[69][70] حتى وقتنا هذا، الأوبئة الناتجة عن الفيروس العجلي B اقتصرت على بر الصين الرئيسي، وأشارات الدراسات الاستقصائية إلى نقص الحصانة لهذا الصنف في الولايات المتحدة الأمريكية.[71]
التاريخ
في 1943، أثبت جيكوب لايت وهوراس هوديس إمكانية ترشيح عامل من براز الأطفال المصابين بالإسهال يسبب أيضاً إسهالًا لدى المواشي.[72] بعد ثلاثة عقود، تبين من العينة المحفوظة أن هذا العامل هو الفيروس العجلي.[73] في السنوات الفاصلة، تبين بأن فيروس لدى الفئران[74] مرتبط بالفيروس المسبب لإسهال الماشية.[75] في 1973، وصفت روث بيشوب وزملائها الفيروسات المرتبطة ببعضها الموجودة لدى الأطفال المصابين بالتهاب المعدة والأمعاء.[76]
في 1974، أقترح توماس هنري فليويت اسم الفيروس العجلي بعد ملاحظته أن، عند معاينته بالمجهر الإلكتروني، اتضح أن جسيم الفيروس العجلي يشبه العجلة (rota في اللاتينية)؛[77][78] اعترفت اللجنة الدولية لتصنيف الفيروسات بالاسم بشكل رسمي بعد أربع سنوات.[79] في 1976، وُجِد فيروسات ذات صلة في عدة أنواع أخرى من الحيوانات.[75] هذه الفيروسات، والتي تسبب جميعها التهابًا معديًا معويًا حادًا، تم الاعتراف بها على أنها مُمرِضات جماعية تصيب البشر والحيوانات حول العالم.[77] الأنماط المصلية للفيروس العجلي وصفت لأول مرة في 1980،[80] وفي العام التالي، نما الفيروس العجلي البشري لأول مرة في مزارع الخلايا المشتقة من كلى القرد، عبر إضافة التربسن (إنزيم موجود في الاثني عشر لدى الثدييات يعرف حاليًا بأنه ضروري للفيروس العجلي ليقوم بعملية النسخ المتماثل) إلى المستنبت.[81] قدرة الفيروس العجلي على النمو في مزارع سرّع سرعة البحث، وبحلول أواسط الثمانينيات تم تقييم اللقاحات الأولى المرشحة.[82]
في 1998، تم ترخيص لقاح للفيروس العجلي لاستعماله في الولايات المتحدة الأمريكية. تجارب إكلينيكية في الولايات المتحدة الأمريكية، وفنلندا، وفنزويلا وجدت بأن اللقاح فعال بنسبة 80 إلى 100% في منع الإسهال الشديد الذي يسببه الفيروس العجلي A، ولم يكتشف الباحثون أي دلالة إحصائية ذات آثار سلبية خطيرة.[83][84] ومع ذلك سحبته الشركة المصنعة من السوق في 1999، بعد اكتشاف أن هذا اللقاح يزيد من خطر الإصابة بالانغلاف المعوي، والذي هو نوع من أنواع الانسداد المعوي، بنسبة واحد لكل 12,000 طفل ملقح.[85] أثارت التجربة نقاشات حادة حول المخاطر النسبية وفوائد لقاح الفيروس العجلي.[86] في 2006، تبينت فعالية لقاحين جديدين ضد عدوى الفيروس العجلي A وأنهما آمنين لدى الأطفال،[87] وفي يونيو 2009 أوصت منظمة الصحة العالمية بإدراج لقاح الفيروس العجلي في جميع برامج التطعيم الوطنية ليمنح الحماية ضد هذا الفيروس.[88]
حيوانات أخرى
الفيروسات العجلية تصيب صغار العديد من الحيوانات وهي مسببات رئيسة للإسهال لدى الحيوانات البرية على مستوى العالم.[7] وبما أنها مُمرِضات في الماشية، لا سيما في العجول والخنازير الصغيرة، تسبب الفيروسات العجلية خسائر اقتصادية لدى المزارعين بسبب تكاليف العلاج المرتبطة بمعدلات مرض ووفاة عالية.[89] هذه الفيروسات العجلية هي مستودعات محتملة للتبادل الجيني مع الفيروسات العجلية البشرية.[90] هناك أدلة بأن الفيروسات العجلية الحيوانية بإمكانها إصابة البشر، إما عبر انتقال الفيروس أو عبر مساهمة عدة قطع RNA بإعادة تشكيل الفيروس بسلاسات تصيب البشر.[91][92]
المراجع
- ^ أ ب Dennehy PH (2000).
- ^ أ ب Bernstein DI (March 2009).
- ^ أ ب Grimwood K, Lambert SB (February 2009).
- ^ ICTV Virus Taxonomy: 2009 Release نسخة محفوظة 10 فبراير 2017 على موقع واي باك مشين.
- ^ أ ب Rheingans RD, Heylen J, Giaquinto C (2006).
- ^ أ ب ت ث ج Simpson E, Wittet S, Bonilla J, Gamazina K, Cooley L, Winkler JL (2007).
- ^ أ ب Edward J Dubovi; Nigel James MacLachlan (2010).
- ^ أ ب Tate JE, Burton AH, Boschi-Pinto C, Steele AD, Duque J, Parashar UD (February 2012). "2008 estimate of worldwide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes: a systematic review and meta-analysis".
- ^ أ ب Fischer TK, Viboud C, Parashar U et al. (2007).
- ^ أ ب Diggle L (2007).
- ^ أ ب Giaquinto C, Dominiak-Felden G, Van Damme P, Myint TT, Maldonado YA, Spoulou V, Mast TC, Staat MA (July 2011).
- ^ Hochwald C, Kivela L (1999).
- ^ Maldonado YA, Yolken RH (1990).
- ^ Glass RI, Parashar UD, Bresee JS, Turcios R, Fischer TK, Widdowson MA, Jiang B, Gentsch JR (July 2006).
- ^ Bishop RF (1996).
- ^ Offit PA (2001).
- ^ Ward R (March 2009).
- ^ Ramsay M and Brown D (2000).
- ^ Hrdy DB (1987).
- ^ Butz AM, Fosarelli P, Dick J, Cusack T, Yolken R (1993).
- ^ Rao VC, Seidel KM, Goyal SM, Metcalf TG, Melnick JL (1 August 1984).
- ^ Kirkwood CD (September 2010).
- ^ O'Ryan M (March 2009).
- ^ Patton JT (January 2012).
- ^ Desselberger U, Wolleswinkel-van den Bosch J, Mrukowicz J, Rodrigo C, Giaquinto C, Vesikari T (2006).
- ^ Greenberg HB, Estes MK (May 2009).
- ^ Greenberg HB, Clark HF, Offit PA (1994).
- ^ Baker M, Prasad BV (2010).
- ^ Jayaram H, Estes MK, Prasad BV (2004).
- ^ Patton JT, Vasquez-Del Carpio R, Spencer E (2004).
- ^ Ruiz MC, Leon T, Diaz Y, Michelangeli F (2009).
- ^ Gregorini, L; Marco, J; Bernies, M; Cassagneau, B; Pomidossi, G; Anguissola, GB; Fajadet, J (Apr 15, 1997).
- ^ Farnworth ER (June 2008).
- ^ Ouwehand A, Vesterlund S (2003).
- ^ Arya SC (1984).
- ^ Patel MM, Tate JE, Selvarangan R et al. (2007).
- ^ The Pediatric ROTavirus European CommitTee (PROTECT) (2006).
- ^ Angel J, Franco MA, Greenberg HB (2009).
- ^ Goode, Jamie; Chadwick, Derek (2001). Gastroenteritis viruses. New York: Wiley. ص. 14. ISBN:0-471-49663-4. مؤرشف من الأصل في 2022-03-27.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Fischer TK, Gentsch JR (2004).
- ^ أ ب ت Jiang V, Jiang B, Tate J, Parashar UD, Patel MM (July 2010).
- ^ O'Ryan M (2007).
- ^ Matson DO (2006).
- ^ Widdowson MA, Steele D, Vojdani J, Wecker J, Parashar U (November 2009).
- ^ Tate JE, Cortese MM, Payne DC, Curns AT, Yen C, Esposito DH, Cortes JE, Lopman BA, Patel MM, Gentsch JR, Parashar UD (January 2011).
- ^ Waggie Z, Hawkridge A, Hussey GD (September 2010).
- ^ Soares-Weiser K, Maclehose H, Bergman H et al. (2012).
- ^ Ward RL, Clark HF, Offit PA (September 2010).
- ^ Tate JE, Patel MM, Steele AD, Gentsch JR, Payne DC, Cortese MM, Nakagomi O, Cunliffe NA, Jiang B, Neuzil KM, de Oliveira LH, Glass RI, Parashar UD (April 2010).
- ^ Moszynski P (2011).
- ^ Alam NH, Ashraf H (2003).
- ^ Sachdev HP (1996).
- ^ Patel MM, Tate JE, Selvarangan R, Daskalaki I, Jackson MA, Curns AT, Coffin S, Watson B, Hodinka R, Glass RI, Parashar UD (أكتوبر 2007). "Routine laboratory testing data for surveillance of rotavirus hospitalizations to evaluate the impact of vaccination". The Pediatric Infectious Disease Journal. ج. 26 ع. 10: 914–9. DOI:10.1097/INF.0b013e31812e52fd. PMID:17901797.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Ramig RF (August 2007).
- ^ Leung AK, Kellner JD, Davies HD (2005).
- ^ UNICEF/WHO (2009) "Diarrhoea: Why children are still dying and what can be done." نسخة محفوظة 07 يونيو 2012 على موقع واي باك مشين.
- ^ Centers for Disease Control and Prevention (CDC) (October 2009).
- ^ Rodrigo C, Salman N, Tatochenko V, Mészner Z, Giaquinto C (May 2010).
- ^ Parashar UD, Gibson CJ, Bresse JS, Glass RI (2006).
- ^ Ryan MJ, Ramsay M, Brown D, Gay NJ, Farrington CP, Wall PG (1996).
- ^ Levy K, Hubbard AE, Eisenberg JN (December 2009).
- ^ Koopmans M, Brown D (1999).
- ^ Anderson EJ, Weber SG (February 2004).
- ^ Hopkins RS, Gaspard GB, Williams FP, Karlin RJ, Cukor G, Blacklow NR (1984).
- ^ Bucardo F, Karlsson B, Nordgren J et al. (2007).
- ^ Linhares AC, Pinheiro FP, Freitas RB, Gabbay YB, Shirley JA, Beards GM (1981).
- ^ Hung T, Chen GM, Wang CG et al. (1984).
- ^ Fang ZY, Ye Q, Ho MS et al. (1989).
- ^ Kelkar SD, Zade JK (2004).
- ^ Ahmed MU, Kobayashi N, Wakuda M, Sanekata T, Taniguchi K, Kader A, Naik TN, Ishino M, Alam MM, Kojima K, Mise K, Sumi A (2004).
- ^ Penaranda ME, Ho MS, Fang ZY et al. (1 October 1989).
- ^ Light JS, Hodes HL (1943).
- ^ Mebus CA, Wyatt RG, Sharpee RL et al. (1 August 1976).
- ^ Rubenstein D, Milne RG, Buckland R, Tyrrell DA (1971).
- ^ أ ب Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB (1 September 1976).
- ^ Bishop R (October 2009).
- ^ أ ب Flewett TH, Woode GN (1978).
- ^ Flewett TH, Bryden AS, Davies H, Woode GN, Bridger JC, Derrick JM (1974).
- ^ Matthews RE (1979).
- ^ Beards GM, Brown DW (March 1988).
- ^ Urasawa T, Urasawa S, Taniguchi K (1981).
- ^ Ward RL, Bernstein DI (January 2009).
- ^ "Rotavirus vaccine for the prevention of rotavirus gastroenteritis among children.
- ^ Kapikian AZ (2001).
- ^ Bines JE (2005).
- ^ Bines J (2006).
- ^ Dennehy PH (2008).
- ^ "Meeting of the immunization Strategic Advisory Group of Experts, April 2009—conclusions and recommendations".
- ^ Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M (January 2010).
- ^ Martella V, Bányai K, Matthijnssens J, Buonavoglia C, Ciarlet M (2010). "Zoonotic aspects of rotaviruses". Veterinary Microbiology. ج. 140 ع. 3–4: 246–55. DOI:10.1016/j.vetmic.2009.08.028. PMID:19781872.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Müller H, Johne R (2007).
- ^ Cook N, Bridger J, Kendall K, Gomara MI, El-Attar L, Gray J (2004).
